题目内容
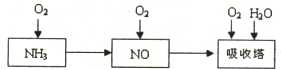 工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:(1)已知反应一经发生,铂铑合金网就会处于红热状态.写出氨催化氧化的化学方程式
(2)硝酸厂尾气常用的处理方法是:
催化还原法:催化剂存在时用H2将NO2还原为N2.
已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
H2O(1)=H2O(g)△H=+44.0kJ/mol
则8g H2恰好将NO2转化成N2和H2O(1)时△H=
(3)氨气是制取硝酸的重要原料,合成氨反应的化学方程式如下:
N2+3H2?2NH3该反应在固定容积的密闭容器中进行.
①下列各项标志着该反应达到化学平衡状态的是
A.容器内N2、H2、NH3的浓度之比为l:3:2
B.3v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的密度保持不变
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2L固定容积的密闭容器中,5min后反应达平衡时,n(N2)=1.2mol,n(H2)=1.2mol,n(NH3)=0.8mol,则反应速率v(N2)=
考点:化学平衡常数的含义,用盖斯定律进行有关反应热的计算,化学平衡的计算
专题:化学平衡专题
分析:(1)在一定条件下氨气与氧气反应生成一氧化氮和水;平衡常数,对于吸热反应,随着温度的升高,K增大,对于放热反应,随着温度的升高,K减小;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,求解;
(3)①根据化学平衡状态的特征分析,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、质量、体积分数以及百分含量不变;
②平衡常数的大小与只与温度有关,与浓度、压强、催化剂无关;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,反应热也处于相应的系数进行相应的加减,求解;
(3)①根据化学平衡状态的特征分析,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、质量、体积分数以及百分含量不变;
②平衡常数的大小与只与温度有关,与浓度、压强、催化剂无关;
解答:
解:(1)氨催化氧化的产物是一氧化氮和水,是工业生产硝酸获得一氧化氮的反应,化学方程式为4NH3+5O2
4NO+6H2O.平衡常数K=
,已知反应一经发生,铂铑合金网就会处于红热状态.可知反应是放热反应,随着温度的升高,K减小;
故答案为:4NH3+5O2
4NO+6H2O,减小;
(2)已知:①2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
②N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
③H2O(1)=H2O(g)△H=+44.0kJ/mol
由盖斯定律可知,①×2-②-4×③,则反应2NO2(g)+4H2(g)=N2(g)+4H2O(l)△H=[2×(-483.6)-67.7-4×44]kJ/mol=-1210.9 kJ/mol,故答案为:-1210.9 kJ/mol;
(3)①A.容器内N2、H2、NH3的浓度之比为l:3:2,取决于起始时各物质的量的关系和转化的程度,不能说明费用达到平衡状态,故A错误;
B.反应达到平衡时,正逆反应速率相等,3v正(N2)=v逆(H2),v正(N2)表示消耗N2的速率,v逆(H2)表示生成H2的速率,且v正(N2):v逆(H2)=1:3,充分说明向两个相反方向进行的程度相当,故B正确;
C.该反应是反应前后气体体积有变化的反应,所以达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,该容器中的压强不再变化时,反应达到平衡状态,故C正确;
D.根据质量守恒,反应前后混合气体的质量不变,容器的体积不变,所以混合气体的密度始终不变,不能证明该反应是否达到平衡状态,故D错误;
故答案为:B、C;
②5分钟后反应达平衡时,n(N2)=1.2mol,n(H2)=1.2mol,n (NH3)=0.8mol,
依据化学平衡三段式列式计算得到;
N2 +3H2 ?2NH3
起始量(mol) 1.6 2.4 0
变化量(mol) 0.4 1.2 0.8
平衡量(mol) 1.2 1.2 0.8
反应速率V(N2)═
=0.04mol/(L?min),平衡时的浓度分别为c(N2)=0.6mol/L、c(H2)=0.6mol/L,c (NH3)=0.4mol/L,则平衡常数K=
=
=1.23;上述平衡体系中的混合气体的浓度增大1倍,相当于缩小体积,则压强增大,化学平衡正向移动,即向右移动;化学平衡常数只与温度有关,与物质的浓度无关;
故答案为:0.04mol?L-1?min-1 ,1.23,向右;
| ||
| △ |
| 生成物平衡浓度幂次方乘积 |
| 反应物平衡浓度幂次方乘积 |
故答案为:4NH3+5O2
| ||
| △ |
(2)已知:①2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
②N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
③H2O(1)=H2O(g)△H=+44.0kJ/mol
由盖斯定律可知,①×2-②-4×③,则反应2NO2(g)+4H2(g)=N2(g)+4H2O(l)△H=[2×(-483.6)-67.7-4×44]kJ/mol=-1210.9 kJ/mol,故答案为:-1210.9 kJ/mol;
(3)①A.容器内N2、H2、NH3的浓度之比为l:3:2,取决于起始时各物质的量的关系和转化的程度,不能说明费用达到平衡状态,故A错误;
B.反应达到平衡时,正逆反应速率相等,3v正(N2)=v逆(H2),v正(N2)表示消耗N2的速率,v逆(H2)表示生成H2的速率,且v正(N2):v逆(H2)=1:3,充分说明向两个相反方向进行的程度相当,故B正确;
C.该反应是反应前后气体体积有变化的反应,所以达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,该容器中的压强不再变化时,反应达到平衡状态,故C正确;
D.根据质量守恒,反应前后混合气体的质量不变,容器的体积不变,所以混合气体的密度始终不变,不能证明该反应是否达到平衡状态,故D错误;
故答案为:B、C;
②5分钟后反应达平衡时,n(N2)=1.2mol,n(H2)=1.2mol,n (NH3)=0.8mol,
依据化学平衡三段式列式计算得到;
N2 +3H2 ?2NH3
起始量(mol) 1.6 2.4 0
变化量(mol) 0.4 1.2 0.8
平衡量(mol) 1.2 1.2 0.8
反应速率V(N2)═
| ||
| 5min |
| 生成物平衡浓度幂次方乘积 |
| 反应物平衡浓度幂次方乘积 |
| 0.42 |
| 0.6×0.63 |
故答案为:0.04mol?L-1?min-1 ,1.23,向右;
点评:本题考查了化学平衡状态的判断、有关化学平衡的计算、盖斯定律的运用等,综合性强,解题时须注意判断平衡状态的标志和角度,计算时须注意方程式中气体的化学计量数关系,题目难度中等.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
下列实验中试剂选用正确的是( )
| A、用稀硝酸与铁反应制取氢气 |
| B、用酒精萃取碘水中的碘 |
| C、用盐酸鉴别苏打和食盐 |
| D、用氢氧化钠溶液与可溶性铝盐制备氢氧化铝 |
对于反应:2H2S+SO2═3S+2H2O,氧化剂与还原剂的分子个数比为( )
| A、1:1 | B、2:1 |
| C、3:1 | D、1:2 |
 .
.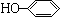 )的电离平衡常数K2的相对大小
)的电离平衡常数K2的相对大小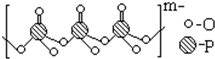

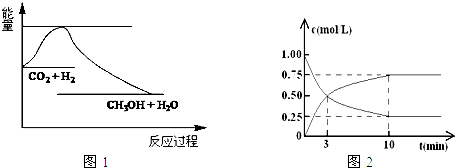
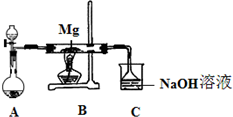 SiO2、SO2和CO2都是酸性氧化物,它们的化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.某兴趣小组用如图所示装置进行Mg与SO2反应的实验.
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性.某兴趣小组用如图所示装置进行Mg与SO2反应的实验.