题目内容
向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2 g。求
①混合物中Cu的质量
②产生的NO在标准状况下的体积
22.(5分) ①12.8 g (3分) ②4.48 L (2分)
【解析】
试题分析:①设Cu、Cu2O的物质的量分别为x、y ,Cu(OH)2的质量为39.2 g,其物质的量为0.4 mol,,则x+2y=0.4 mol,64 g·mol-1·x+144 g·mol-1·y=27.2 g,解得x=0.2 mol,y=0.1 mol,混合物中Cu的质量为0.2molx64g?mol-1=12.8g
②Cu和Cu2O中的Cu都变成了+2价,转移的电子的物质的量为(0.4+0.2)mol=0.6 mol,根据得失电子守恒可知,生成的NO应为0.2 mol,产生的NO在标准状况下的体积为0.2x22.4=4.48 L.
考点:考查氧化还原反应的计算。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO 3都能被碱石灰和氢氧化钠溶液吸收。用下图装置加热硫酸铜粉末直至完全分解。若硫酸铜粉末质量为10.0 g,完全分解后,各装置的质量变化关系如下表所示。
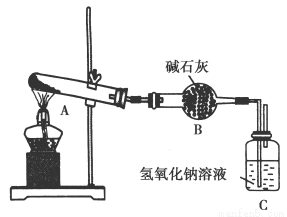
装置 | A(试管+粉末) | B | C |
反应前 | 42.0 g | 75.0 g | 140.0 g |
反应后 | 37.0 g | 79.5 g | 140.0 g |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是
A.4CuSO4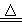 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑
B.3CuSO4 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑
C.5CuSO4 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑
D.6CuSO4 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
 eC(气)+dD(气) △H<0,下列能证明该反应一定达到平衡状态的是
eC(气)+dD(气) △H<0,下列能证明该反应一定达到平衡状态的是