题目内容
8. 碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题:
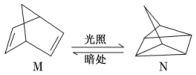
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题:(1)有机物M经过太阳光光照可转化成N,转化过程如下:
△H=+88.6kJ/mol,则M、N相比,较稳定的是M.
(2)已知CH3OH(l)的燃烧热△H=-238.6kJ/mol,CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-a kJ/mol,则a<238.6(填“>”“<”或“=”).
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1.
(4)火箭和导弹表面的薄层是耐高温物质.将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为98kJ.
(5)汽车排出的尾气中含有CO和NO等气体.为了解决污染问题,在汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物CO和NO转化为无毒的大气循环物质.已知:
N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol
2C(s)+O2(g)═2CO(g)△H=-221.0kJ/mol
C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
请写出污染物CO和NO转化为无毒的大气循环物质的热化学方程式是:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJ/mol.
分析 (1)M转化为N是吸热反应,所以N的能量高,不稳定;
(2)甲醇燃烧生成CO2(g)和H2(g)属于不完全燃烧,放出的热量少,故a<238.6;
(3)根据热化学方程式的含义和书写方法来回答;
(4)所给反应中转移12个电子,故每转移1mol电子放出的热量为1 176kJ÷12=98kJ;
(5)N2(g)+O2(g)═2NO(g);△H=+180.5kJ/mo1①
2C(s)+O2(g)═2CO(g);△H=-221.0kJ/mo1②
C(s)+O2(g)═CO2(g);△H=-393.5kJ/mo1③
根据盖斯定律可得:③×2-①-②,由此分析解答.
解答 解:(1)有机物M经过太阳光光照可转化成N,:△H=+88.6kJ•mol-1,过程是吸热反应,N暗处转化为M,是放热反应,能量越低越稳定,说明M稳定;
故答案为:M;
(2)燃烧热是1mol物质完全燃烧生成稳定氧化物放出的热量,甲醇燃烧生成CO2(g)和H2(g)属于不完全燃烧,放出的热量小于燃烧热,
故答案为:<;
(3)1molCl2参与反应时释放出145KJ热量,则反应2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)会放出290KJ的能量,即2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1,
故答案为:2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0 kJ•mol-1;
(4)4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1176kJ•mol-1,转移12mol电子放热1176KJ,则反应过程中,每转移1mol电子放热98kJ,
故答案为:98kJ;
(5)N2(g)+O2(g)═2NO(g);△H=+180.5kJ/mo1①
2C(s)+O2(g)═2CO(g);△H=-221.0kJ/mo1②
C(s)+O2(g)═CO2(g);△H=-393.5kJ/mo1③
根据盖斯定律可得:③×2-①-②,2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5 kJ•mol-1,
故答案为:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5kJ/mol.
点评 本题考查了化学反应能量变化,燃烧热概念分析判断,氧化还原反应电子转移的计算应用,掌握基础是解题关键,题目难度中等.

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案| A. | 葡萄糖制镜利用了葡萄糖的氧化性 | |
| B. | 室温下,在水中的溶解度:乙醇>苯酚>乙酸乙酯 | |
| C. | 酯在碱性条件下水解生成对应的酸和醇 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,说明甲基使苯环变活泼 |
| A. | 22.4LNH3分子中含有3NA个N-H键 | |
| B. | 2.3 g Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA | |
| C. | 1 L0.1 mol•L-1蔗糖溶液中所含分子数为0.1NA | |
| D. | 常温常压下,46g NO2含有的原子数小于3NA |
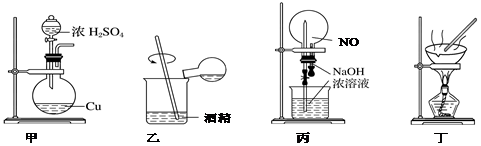
| A. | 用图甲做铜与浓硫酸反应制取SO2 | |
| B. | 用图乙配制浓硫酸与酒精的混合液 | |
| C. | 用图丙做NO与NaOH溶液的“喷泉”实验 | |
| D. | 用装置丁做蒸发CuCl2溶液获得CuCl2•2H2O |
【提出假设】
假设1:沉淀为CuCO3;
假设2:沉淀为Cu(OH)2;
假设3:沉淀为碱式碳酸铜[化学式可表示为nCu(OH)2•mCuCO3].
【查阅资料】这三种沉淀受热均易分解,都生成黑色固体CuO.
【实验探究】
步骤1:将所得悬浊液过滤,先用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:取一定量所得固体,用如图装置(夹持仪器未画)进行定性实验;
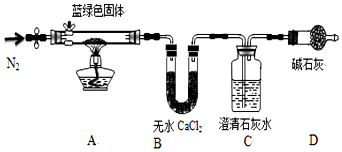
【问题讨论】
(1)假设2中的沉淀为Cu(OH)2,提出该假设的理论依据是碳酸根水解,溶液中含有较多的OH-
(2)步骤1用无水乙醇洗涤,再风干的目的利用乙醇的易挥发,带走洗涤的水;
(3)装置D装有碱石灰的干燥管所起的作用是利用乙醇的易挥发,带走洗涤的水
(4)若反应后A中蓝绿色固体变黑,C中澄清石灰水变浑浊,证明假设假设2(填写序号)一定不成立
(5)乙同学认为只要将图中B装置的试剂改用下列某试剂后,通过观察便可验证上述所有假设,该试剂是b(填代号)
a.浓硫酸 b.无水CuSO4 c.碱石灰 d.P2O5
(6)该小组经试验确定假设3成立,他们想进一步测定蓝绿色固体的化学式,丙同学查得一些物质在20℃的数据(如下表)后,建议将C中的澄清石灰水改为Ba(OH)2溶液,其原因是ac(双选,填代号)
| 溶解度(s)/g | 溶度积(Ksp) | 摩尔质量(M)g/mol | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
b.Ba(OH)2为强碱,Ca(OH)2为弱碱
c.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
d.相同条件下,CaCO3的溶解度明显大于BaCO3
(7)作上述调整后,若所取蓝绿色固体质量为27.1g,实验结束后装置B中无水氯化钙的质量增加2.7g,C中氢氧化钡溶液里产生沉淀的质量为19.7g.则该蓝绿色固体的化学式为2CuCO3•3Cu(OH)2或3Cu(OH)2•2CuCO3或Cu5(OH)6(CO3)2.
①将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-5 | 6×10-5 | 2×10-4 | 4×10-4 | 3×10-4 | 2×10-4 |
②汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图3:
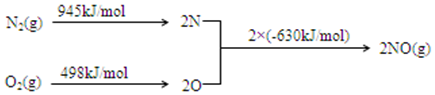
则:NO(g)?$\frac{1}{2}$N2(g)+$\frac{1}{2}$O2(g)△H=-91.5kJ•mol-1.
| A. | 乙烷与氯气光照反应可以制得较纯净的1,2-二氯乙烷 | |
| B. | 苯中的化学键都是非极性键 | |
| C. | 煤的干馏属于物理变化 | |
| D. | 涤纶、酚醛树脂和蛋白质都属于高分子化合物 |
| A. | 原子半径逐渐增大 | |
| B. | 单质氧化性逐渐增强 | |
| C. | 气态氢化物的稳定性逐渐增强 | |
| D. | 都有最高价氧化物的水化物,化学式为HXO4 |
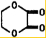 +2H2O;
+2H2O;