题目内容
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B、熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C、NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |
| D、NCl3分子中所有的原子均为8电子稳定结构 |
考点:元素周期律的作用,不同晶体的结构微粒及微粒间作用力的区别
专题:
分析:A.元素的非金属性越强,气体氢化物的热稳定性越强;HF中含有氢键,故熔沸点较高;
B.熔融状态下能导电的化合物为离子化合物;金属与非金属元素形成的化合物不一定是离子化合物;
C.NaHSO4晶体中阴离子为硫酸氢根离子,阳离子为钠离子,个数是1:1,熔化时破坏的是离子键;
D.NCl3分子中N原子与3个氯原子共用3对共用电子对,故所有的原子均为8电子稳定结构.
B.熔融状态下能导电的化合物为离子化合物;金属与非金属元素形成的化合物不一定是离子化合物;
C.NaHSO4晶体中阴离子为硫酸氢根离子,阳离子为钠离子,个数是1:1,熔化时破坏的是离子键;
D.NCl3分子中N原子与3个氯原子共用3对共用电子对,故所有的原子均为8电子稳定结构.
解答:
解:A.非金属性:F>Cl>Br>I,故HF、HCl、HBr、HI的热稳定性依次减弱;HF中含有氢键,故熔沸点较高,故沸点:HF>HI>HBr>HCl,故A错误;
B.熔融状态下能导电的化合物为离子化合物,故一定含离子键;金属与非金属元素形成的化合物不一定是离子化合物,如氯化铝是共价化合物,故B错误;
C.NaHSO4晶体中阴离子为硫酸氢根离子,阳离子为钠离子,个数是1:1,熔化时破坏的是离子键,故C错误;
D.NCl3分子中N原子与3个氯原子共用3对共用电子对,故所有的原子均为8电子稳定结构,故D正确;
故选D.
B.熔融状态下能导电的化合物为离子化合物,故一定含离子键;金属与非金属元素形成的化合物不一定是离子化合物,如氯化铝是共价化合物,故B错误;
C.NaHSO4晶体中阴离子为硫酸氢根离子,阳离子为钠离子,个数是1:1,熔化时破坏的是离子键,故C错误;
D.NCl3分子中N原子与3个氯原子共用3对共用电子对,故所有的原子均为8电子稳定结构,故D正确;
故选D.
点评:本题考查元素周期律的作用、氢键的性质、离子晶体与分子晶体的构成微粒与微粒间的作用力分析,难度中等.要注意基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法错误的是( )
| A、NH4NO3 溶于水虽然吸热,但其溶于水是自发过程 |
| B、加热液体(温度高于沸点)会自发转变成气体,可用熵变解释 |
| C、同温同压下,H2(g)+Cl2(g)?2HCl(g)在光照和点燃条件下的△H不同 |
| D、要正确判断化学反应能否自发进行,要综合考虑反应的△H和△S |
下列化学反应中,既是离子反应,又是氧化还原反应的是( )
| A、2NaOH+H2SO4═Na2SO4+2H2O |
| B、Fe+H2SO4═FeSO4+H2↑ |
| C、BaCl2+H2SO4═BaSO4↓+2HCl |
| D、H2+CuO═Cu+H2O |
已知H++OH-═H2O生成1mol H2O放出热量57.3kJ,下列反应中能放出57.3kJ热量的是( )
| A、1mol稀H2SO4与足量NaOH溶液反应 |
| B、稀盐酸与氨水反应生成1 mol H2O |
| C、稀NaOH与95%浓硫酸反应生成1 mol水 |
| D、稀盐酸与稀Ba(OH)2溶液反应生成1 mol水 |
1mol 某元素的单质直接与氯气反应后,质量增加7.1g,这种元素是( )
| A、Na | B、Mg | C、Fe | D、Al |
想一想:Ba(OH)2(液态)、CuSO4(固态)、纯CH3COOH这些物质为什么归为一类,下列哪些物质还可以和它们归为一类( )
| A、医用酒精 | B、HCl(气态) |
| C、水煤气 | D、豆浆 |
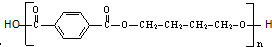 )是一种重要的工程塑料.
)是一种重要的工程塑料.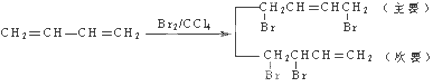
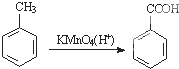
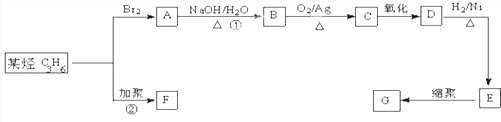
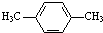 为原料合成PBT(请用反应流程图表示,并注明反应条件).示例:由乙醇合成聚乙烯的反应流程图可表示为CH3CH2OH
为原料合成PBT(请用反应流程图表示,并注明反应条件).示例:由乙醇合成聚乙烯的反应流程图可表示为CH3CH2OH 合成PBT的反应流程图为:
合成PBT的反应流程图为: