题目内容
10.密度为1.45g/cm3的硫酸溶液中,逐滴加入BaCl2溶液,直至沉淀完全为止,过滤,已知滤液与原BaCl2溶液的质量相等,则原硫酸溶液的物质的量浓度为( )| A. | 3.2mol/L | B. | 6.2mol/L | C. | 14.8mol/L | D. | 18.4mol/L |
分析 硫酸溶液与氯化钡溶液反应BaCl2+H2SO4═BaSO4↓+2HCl,假设原硫酸溶液的质量,则沉淀硫酸钡质量与原硫酸溶液质量相等,计算出硫酸溶液体积,根据化学方程式计算出硫酸溶液中H2SO4的物质的量,再由c=$\frac{n}{V}$计算.
解答 解:令硫酸溶液的质量为233g,由于硫酸溶液的质量=硫酸钡的质量,则硫酸钡的质量为233g,
所以硫酸溶液体积为$\frac{233g}{1450g/L}$=$\frac{233}{1450}$L
设硫酸溶液中溶质的物质的量为x,则:
BaCl2+H2SO4═BaSO4↓+2HCl
1mol 233g
x 233g
所以x=1mol,
所以原的硫酸溶液中溶质的物质的量浓度为$\frac{1mol}{\frac{233}{1450}L}$=6.2mol/L,
故选:B.
点评 本题考查物质的量浓度计算,属于无数据计算,理解物质的量浓度定义式是关键,注意利用特值方法解答,难度中等,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
16.下列仪器名称为“蒸馏烧瓶”的是( )
| A. | 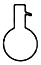 | B. |  | C. |  | D. | 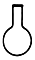 |
1.下列化工生产过程中,未涉及氧化还原反应的是( )
| A. | 海带提碘 | B. | 氯碱工业 | C. | 海水提溴 | D. | 侯德榜制碱法 |
18.下列关于氯气及其组成的说法正确的是( )
| A. | 氯气有毒,不能吸入不能闻 | B. | 氯元素呈黄绿色 | ||
| C. | 氯离子、氯原子都是氯元素 | D. | 氯气有漂白性 |
5.下列名称与化学式表示同一物质的是( )
| A. | 明矾FeSO4•7H2O | B. | 石膏Na2SO4•10H2O | ||
| C. | 重晶石Na2CO3•10H2O | D. | 胆矾CuSO4•5H2O |
15.下列物质的水溶液不能电离出Cl-的是( )
| A. | HCl | B. | NaClO | C. | MgCl2 | D. | NaCl |
19.下列说法正确的是( )
| A. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| B. | 植物油的主要成分是高级脂肪酸 | |
| C. | 蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖 | |
| D. | 食用白糖的主要成分是蔗糖 |