题目内容
17.(1)自来水厂用氯气进行消毒,改善水质,因为氯气与水反应会生成盐酸和次氯(HClO)次氯酸具有杀菌消毒作用,其反应方程式为:Cl2+H2O═HCl+HClO(2)氯气与氢氧化钙溶液反应能制得漂白粉(次氯酸钙与氯化钙的混合物).试写出反应的化学方式:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
分析 (1)氯气与水反应会生成盐酸和次氯(HClO),以此书写反应方程式;
(2)氯气与氢氧化钙溶液反应能制得漂白粉(次氯酸钙与氯化钙的混合物),以此书写反应方程式.
解答 解:(1)氯气与水反应会生成盐酸和次氯(HClO),反应方程式为:Cl2+H2O═HCl+HClO,
故答案为:Cl2+H2O═HCl+HClO;
(2)氯气与氢氧化钙溶液反应能制得漂白粉,生成次氯酸钙、氯化钙和水,反应方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
点评 本题考查化学反应方程式的书写,明确发生的化学反应的产物是解答的关键,注重物质的性质及化学用语的考查,题目较简单.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
7.在体积均为1.0L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1mol CO2和0.2mol CO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
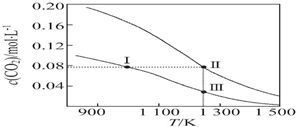

| A. | 反应CO2(g)+C(s)═2CO(g)的△S>0、△H<0 | |
| B. | 体系的总压强p总:p总(状态Ⅱ)>2p总(状态Ⅰ) | |
| C. | 体系中c(CO):c(CO,状态Ⅱ)>2c(CO,状态Ⅲ) | |
| D. | 逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ) |
8.将盛有amolNO2和bmolNO混合气体的试管倒立于水槽中,再通人bmolO2充分反应后试管里剩余气体的成分及物质的量决定于a与b的关系,请填写表格:
| a与b的关系 | 剩余气体的成分 | 剩余气体物质的量 |
| 若a=b | ||
| 若a>b | ||
| 若a<b |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2L苯中所含的分子数为0.5NA | |
| B. | 标准状况下,22.4L O2与44.8L SO2充分反应后转移电子的数目为4NA | |
| C. | 各为0.1mol的H3O+和OH-中含有的电子数目均为0.9NA | |
| D. | 2.4g O2和O3的组成的混合气体中所含的氧原子数目为0.15NA |
9.金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称.下列有关${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的说法正确的是( )
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti 原子中均含22个中子 | |
| B. | 分别由${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti 组成的金属钛单质互称同分异构体 | |
| C. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti 在周期表中位置相同,都在第四周期 | |
| D. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti为同一核素 |
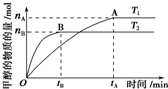 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ,•mol-1.(注:燃烧热:1mol燃料完全燃烧所放出的能量即为该燃料的燃烧热.)请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ,•mol-1.(注:燃烧热:1mol燃料完全燃烧所放出的能量即为该燃料的燃烧热.)请回答下列问题: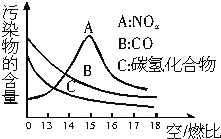 稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,现用的汽油尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如图所示.
稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧.随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,现用的汽油尾气净化装置不能有效地将NOx转化为N2.不同空/燃比时汽车尾气中主要污染物的含量变化如图所示.