题目内容
已知2SO (g)+O
(g)+O (g)
(g)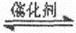 2SO
2SO (g) △H=-197 kJ·mol
(g) △H=-197 kJ·mol 。向同温、同体积的三个密闭容器中分别通入气体:(甲)2mol SO
。向同温、同体积的三个密闭容器中分别通入气体:(甲)2mol SO 和1mol O
和1mol O ;(乙)1mol SO
;(乙)1mol SO 和0.5mol O
和0.5mol O ;(丙)2mol SO3。恒温恒容下反应达到平衡时,下列关系一定正确的是
;(丙)2mol SO3。恒温恒容下反应达到平衡时,下列关系一定正确的是
A.容器内压强p:p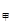 =p =p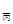 >2p >2p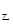 |
B.SO 的质量m:m 的质量m:m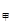 =m =m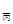 >2m >2m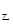 |
C.c(SO )与c(O )与c(O )之比k:k )之比k:k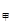 =k =k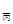 >k >k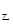 |
D.反应放出或吸收的热量的数值Q:Q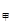 =Q =Q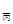 >2Q >2Q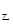 |
B
解析试题分析:根据题意可知甲和丙容器是等效的,乙容器相当于扩大容器为原来的一半,所以乙容器在减小压强的过程中平衡逆向移动,压强比原来的一半大,所以p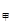 =p
=p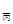 <2p
<2p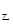 ,SO3的质量比原来的一半小,所以m
,SO3的质量比原来的一半小,所以m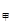 =m
=m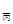 >2m
>2m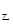 ,c(SO
,c(SO )与c(O
)与c(O )之比k不变,所以k
)之比k不变,所以k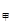 =k
=k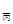 =k
=k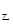 ,放出的热量比原来的一半小,所以Q
,放出的热量比原来的一半小,所以Q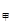 >2Q
>2Q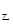 ,Q甲+Q丙=197,所以正确的是B。答案选B。
,Q甲+Q丙=197,所以正确的是B。答案选B。
考点:化学等效平衡
点评:本题的关键是甲乙容器的比较,乙容器相当于甲容器扩大体积为原来的一半,然后再进行比较。

练习册系列答案
相关题目
 (g)+O
(g)+O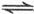 2SO
2SO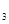 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO