题目内容
下列各装置中铜电极上能产生气泡的是( )
A、 |
B、 |
C、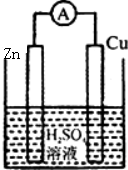 |
D、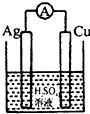 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:铜电极上产生气泡,说明该装置能构成原电池,且铜作正极,根据原电池的构成条件判断即可.
解答:
解:A.乙醇溶液不是电解质溶液,该装置不能发生任何反应,也不能形成原电池,故A错误;
B.该装置两个电极材料相同,不能构成原电池,故B错误;
C.该装置符合原电池的构成条件,锌比铜活泼,失电子作负极,铜作正极,正极上氢离子得电子生成氢气,故C正确;
D.该装置没有自发进行氧化还原反应,不能构成原电池,故D错误;
故选C.
B.该装置两个电极材料相同,不能构成原电池,故B错误;
C.该装置符合原电池的构成条件,锌比铜活泼,失电子作负极,铜作正极,正极上氢离子得电子生成氢气,故C正确;
D.该装置没有自发进行氧化还原反应,不能构成原电池,故D错误;
故选C.
点评:本题考查了原电池构成条件,明确原电池构成条件是解本题关键,原电池构成条件是:该反应是自发进行的、放热的、氧化还原反应,有两个活泼性不同的电极,电极必须插入电解质溶液中,且形成闭合回路.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
25℃时,Ksp(BaSO4)=1×10-10,Ksp (BaCO3)=2.6×10-9.该温度下,下列说法不正确的是( )
| A、同浓度的Na2SO4和Na2CO3混合溶液中滴加BaCl2溶液,BaSO4先析出 | ||||||||
| B、BaCO3的悬浊液中加入少量的新制氯水,c(Ba2+)增大 | ||||||||
C、BaSO4和BaCO3共存的悬浊液中
| ||||||||
| D、BaSO4悬浊液中加入Na2CO3浓溶液,BaSO4不可能转化为BaCO3 |
下列离子方程式书写正确的是( )
| A、Fe3O4溶于稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| B、铝片溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| C、向苯酚钠溶液中通入少量CO2;C6H5O-+CO2+H2O→C6H5OH+HCO3- |
| D、向含1mol碘化亚铁的溶液中通入标准状况下22.4L氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
下列说法正确的是( )
| A、两种难溶电解质作比较时,Ksp越小溶解度越小 |
| B、欲使溶液中某离子沉淀完全,加入的沉淀剂越多越好 |
| C、所谓沉淀完全就是用沉淀剂将溶液中某一离子除净 |
| D、温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp时,此溶液为AgCl的饱和溶液 |
在固定容积的容器中盛有1mol PCl5,200℃时发生如下反应:PCl5(g)?PCl3+Cl2(g)达到平衡时,PCl5体积分数为M%.若在同一温度和同一容器中,最初投入2molPCl5,达平衡时,PCl5所占体积分数为N%,则M和N的关系是( )
| A、M<N | B、M>N |
| C、M=N | D、无法比较 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)=c(H+) |
| B、在0.1 mol?L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| C、已知叠氮酸(HN3)与醋酸酸性相近,则在NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(OH?)>c(N3?)>c(H+) |
| D、0.2 mol?L-1NaHCO3溶液中加入等体积0.1 mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
 Ⅰ.依据氧化还原反应:2Ag+(aq)+Cu (s)=Cu2+(aq)+2Ag(s) 设计的原电池如图所示.请回答:
Ⅰ.依据氧化还原反应:2Ag+(aq)+Cu (s)=Cu2+(aq)+2Ag(s) 设计的原电池如图所示.请回答: 合成氨工业的出现大大缓解了人类粮食危机,合成氨工业的核心反应是:N2+3H2
合成氨工业的出现大大缓解了人类粮食危机,合成氨工业的核心反应是:N2+3H2