题目内容
5.下列物质各3g,在氧气中完全燃烧,于150℃时将产物通过足量的Na2O2固体后,固 体增重大于3g的是( )| A. | HCOOH | B. | CH3COOH | C. | C2H5OH | D. | C6H12O6 |
分析 水、二氧化碳和Na2O2反应方程式分别为2H2O+2Na2O2=4NaOH+O2、2Na2O2+2CO2=2Na2CO3+O2,根据方程式知,水和Na2O2反应时固体质量增加量相当于H2质量,二氧化碳和Na2O2反应时固体质量增加量相当于CO质量,将可燃物写出H2或CO或(CO)m•Hn方式,如果恰好写为H2或CO或(CO)m•Hn方式,则产物通过足量Na2O2时固体质量不变,如果改写化学式时O原子有剩余,则反应前后固体质量减少,如果C原子有剩余,则固体质量增加,据此分析解答.
解答 解:水、二氧化碳和Na2O2反应方程式分别为2H2O+2Na2O2=4NaOH+O2、2Na2O2+2CO2=2Na2CO3+O2,根据方程式知,水和Na2O2反应时固体质量增加量相当于H2质量,二氧化碳和Na2O2反应时固体质量增加量相当于CO质量,将可燃物写出H2或CO或(CO)m•Hn方式,如果恰好写为H2或CO或(CO)m•Hn方式,则产物通过足量Na2O2时固体质量不变,如果改写化学式时O原子有剩余,则反应前后固体质量减少,如果C原子有剩余,则固体质量增加;
A.HCOOH可以改写成CO•H2•O,O原子有剩余,所以反应前后固体质量增多少于3g,不符合,故A不选;
B.该化学式可以改写为(CO)2•(H2)2,所以反应前后固体质量增多等于3g,不符合,故B不选;
C.该化学式可以改写为CO•(H2)3•C,C有剩余,则反应前后固体质量增多多于3g,符合,故C选;
D.该化学式可以改写为(CO)6•(H2)6,则反应前后固体质量增多等于3g,故不符合,故D不选.
故选C.
点评 本题考查化学方程式有关计算,明确反应前后固体质量增加成分是解本题关键,利用化学式分析判断即可,注意解题方法技巧,题目难度中等.

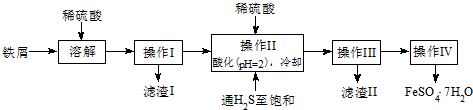
查询资料,得有关物质的数据如表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
A.KSCN溶液 B.NaOH溶液 C.KMnO4溶液
(2)操作II中,通入硫化氢至饱和的目的是除去溶液中的Sn2+离子,并防止Fe2+被氧化.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(5)测定绿矾产品中Fe2+含量的方法是:
a.称取一定量的绿矾产品,溶解,在250mL容量瓶中定容;b.量取一定量的待测溶液于锥形瓶中;c.再用硫酸酸化的KMnO4溶液滴定至终点.
①滴定时盛放KMnO4溶液的仪器为酸式滴定管(填仪器名称).
②判断此滴定实验达到终点的方法是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色.
| A. | Na+、K+、CO32-、NO3- | B. | Mg2+、NH4+、SO42-、Cl- | ||
| C. | Fe3+、K+、NO3-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
| A. | 2倍 | B. | 1.5倍 | C. | 0.9倍 | D. | 0.5倍 |
| A. | 用食醋除水垢 | |
| B. | 甘油加水作护肤剂 | |
| C. | 双氧水漂白美容 | |
| D. | 烹鱼时,加入少量的料酒和食醋可减少腥味,增加香味 |
| A. | 1mol葡萄糖可水解生成2mol乳酸(C3H6O3) | |
| B. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| C. |  nOH的结构中含有酯基 nOH的结构中含有酯基 | |
| D. | 油脂和蛋白质都是能发生水解反应的高分子化合物 |
| A. | CH4(g)+2O2(g)=CO2(g)+4H2O(g)△H=-890 kJ/mol | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890 kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+H2O(l)△H=-445 kJ/mol | |
| D. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890 kJ/mol |