题目内容
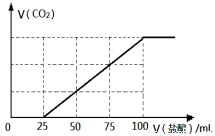
向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是
A.原NaOH溶液的浓度为0.2 mol/L
B.通入CO2的体积为448 mL
C.所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3) = 1: 3
D.所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) = 1: 1
A
【解析】
试题分析:当向100mLNaOH溶液中通入一定量的CO2气体时,充分反应后发生的反应有:2NaOH+CO2═Na2CO3+H2O或NaOH+CO2═NaHCO3两种可能情况,在加入盐酸100mL时,无论NaOH 、NaHCO3还是Na2CO3都会生成NaCl,根据化学反应中原子守恒,则有n(Na+)=n(Cl-)所以n(NaOH)=n(HCl)=0.02moL,NaOH和盐酸的体积相同,那么浓度也相同,即原NaOH溶液的浓度为0.2 mol/L,A正确;体积必须在标准状况下测定,B错误;盐酸由25mL滴至100mL时,发生的反应为NaHCO3+HCl=NaCl+CO2+H2O消耗盐酸0.015moL,生成CO2 0.015moL,设所得溶液中的Na2CO3 为ⅹmoL NaHCO3为y moL,根据原子守恒:2ⅹ+y=0.02 ; x+y=0.015解得x=0.005 y=0.01所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3) = 2: 1,C、D都错误。
考点:考察元素化合物的性质及定量运算。

练习册系列答案
相关题目
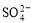 离子有一部分是氧化产物
离子有一部分是氧化产物 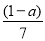 B.
B.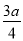 C.
C.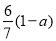 D.
D.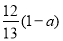
 5Ca2+(aq)+3PO43-(aq)+OH- (aq) Ksp = 6.8×10-37
5Ca2+(aq)+3PO43-(aq)+OH- (aq) Ksp = 6.8×10-37 -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )