题目内容
把13g含有SiO2的CaCO3固体在高温下加热到质量不再减少为止,冷却后剩余固体称重为8.6g.回答下列问题:
(1)生成的CO2在标准状况下的体积为 L.
(2)求原物质中含SiO2的质量.
(3)计算剩余固体中各成分的质量.
(1)生成的CO2在标准状况下的体积为
(2)求原物质中含SiO2的质量.
(3)计算剩余固体中各成分的质量.
考点:化学方程式的有关计算
专题:计算题
分析:(1)可能发生的反应为:SiO2+CaCO3═CaSiO3+CO2↑、CaCO3═CaO+CO2↑,无论怎样反应,CaCO3均转化为CO2,固体减小质量为二氧化碳质量,计算二氧化碳的物质的量,根据V=nVm计算其体积;
(2)根据碳原子守恒计算n(CaCO3),进而二氧化硅的质量;
(3)假设二氧化硅完全转化为硅酸钙,根据方程式计算硅酸钙的质量,根据Ca元素守恒确定剩余固体否含有CaO或SiO2,进而计算各成分的质量.
(2)根据碳原子守恒计算n(CaCO3),进而二氧化硅的质量;
(3)假设二氧化硅完全转化为硅酸钙,根据方程式计算硅酸钙的质量,根据Ca元素守恒确定剩余固体否含有CaO或SiO2,进而计算各成分的质量.
解答:
解:(1)可能发生的反应为:SiO2+CaCO3═CaSiO3+CO2↑、CaCO3═CaO+CO2↑,无论怎样反应,CaCO3均转化为CO2,故m(CO2)=13g-8.6g=4.4g,n(CO2)=
=0.1 mol,则:生成的CO2在标准状况下的体积为0.1mol×22.4L/mol=2.24L,
故答案为:2.24;
(2)根据碳原子守恒:n(CaCO3)=n(CO2)=0.1 mol,则:m(CaCO3)=10g,m(SiO2)=13g-10g=3g,
答:原物质中含SiO2的质量为3g;
(3)假设二氧化硅完全转化为硅酸钙,则:
SiO2~CaSiO3
60g 116g
3g m(CaSiO3)
所以,m(CaSiO3)=
=5.8g,n(CaSiO3)=
=0.05mol,
由Ca元素守恒可知,剩余固体中含有CaO,则m(CaO)=8.6g-5.8g=2.8g,
答:剩余固体中CaSiO3为5.8g,CaO为2.8g.
| 4.4g |
| 44g/mol |
故答案为:2.24;
(2)根据碳原子守恒:n(CaCO3)=n(CO2)=0.1 mol,则:m(CaCO3)=10g,m(SiO2)=13g-10g=3g,
答:原物质中含SiO2的质量为3g;
(3)假设二氧化硅完全转化为硅酸钙,则:
SiO2~CaSiO3
60g 116g
3g m(CaSiO3)
所以,m(CaSiO3)=
| 3g×116g |
| 60g |
| 5.8g |
| 116g/mol |
由Ca元素守恒可知,剩余固体中含有CaO,则m(CaO)=8.6g-5.8g=2.8g,
答:剩余固体中CaSiO3为5.8g,CaO为2.8g.
点评:本题考查混合物计算、化学方程式计算,难度不大,注意利用过量计算确定剩余物质的组成.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
我国最近报道的高温超导体材料中,铊(Tl)是其成分之一,已知铊与铝是同族元素,关于铊的性质判断中,可能错误的是( )
| A、铊是银白色金属 |
| B、Tl(OH)3和Al(OH)3一样是两性氢氧化物 |
| C、能形成+3价的化合物 |
| D、与稀硝酸作用生成硝酸盐 |

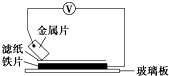 将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表所示:
将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表所示: