题目内容
下列叙述正确的是( )
| A、1 mol H2O的质量为18g/mol |
| B、3.01×1023个SO2分子的质量为32g |
| C、氧的摩尔质量为16g/mol |
| D、标准状况下,1 mol任何物质体积均为22.4L |
考点:物质的量的相关计算
专题:计算题
分析:A.质量的单位是g;
B.n(SO2)=
=0.5mol,气体质量m=nM;
C.摩尔质量单位是g/mol,且指代不明确;
D.标况下,1mol任何气体体积都约为22.4L.
B.n(SO2)=
| 3.01×1023 |
| 6.02×1023/mol |
C.摩尔质量单位是g/mol,且指代不明确;
D.标况下,1mol任何气体体积都约为22.4L.
解答:
解:A.质量的单位是g,1 mol H2O的质量=1mol×18g/mol=18g,故A错误;
B.n(SO2)=
=0.5mol,气体质量m=nM=0.5mol×64g/mol=32g,故B正确;
C.摩尔质量单位是g/mol,且指代不明确,氧原子的摩尔质量是16g/mol,故C错误;
D.气体体积受温度和压强影响,液体和固体不受温度和压强影响,所以标况下,1mol任何气体体积都约为22.4L,故D错误;
故选B.
B.n(SO2)=
| 3.01×1023 |
| 6.02×1023/mol |
C.摩尔质量单位是g/mol,且指代不明确,氧原子的摩尔质量是16g/mol,故C错误;
D.气体体积受温度和压强影响,液体和固体不受温度和压强影响,所以标况下,1mol任何气体体积都约为22.4L,故D错误;
故选B.
点评:本题考查物质的量的有关计算,知道质量、摩尔质量单位,注意气体摩尔体积适用范围及适用条件,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组离子,在指定的环境中能大量共存的是( )
| A、在中性的溶液中:Ag+、K+、SO42-、Cl- |
| B、pH=12的溶液中:Na+、S2-、AlO2-、SO32- |
| C、有CO32-存在的溶液中:Na+、Fe3+、Ca2+、I- |
| D、在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- |
短周期主族元素X、Y、Z、W在元素周期表中的位置关系如图,下列推论合理的是( )
| X | Y |
| W | Z |
| A、若Z的核电荷数是Y的两倍,则X为碳元素 |
| B、若W的核电荷数是Y的两倍,则X是氮元素 |
| C、原子半径:Z>Y>X |
| D、最简单氢化物的稳定性:Y>X>W |
下列说法正确的是( )
A、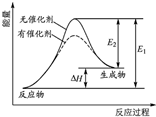 某反应的反应过程中能量变化如图所示,由如图分析可知催化剂不改变反应的焓变 | ||||||||||
| B、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | ||||||||||
C、已知:
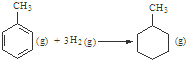 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 | ||||||||||
| D、常温下在0.10 mol?L-1的氨水中加入少量NH4Cl晶体,NH3?H2O的电离程度和溶液的pH均减小 |
NA代表阿伏加德罗常数的数值.下列说法中正确的是( )
| A、在1L0.1mol/L碳酸钠溶液中,阴离子总数大于0.1 NA |
| B、1molCaC2中含有阴离子数目为2NA |
| C、120gNaHSO4在水溶液和熔融状态下电离出来的离子总数均为3NA |
| D、2mol SO2和1 mol O2混合气体在V2O5存在的条件下于密闭容器中加热反应后容器内物质分子数小于2NA |