题目内容
固体A和B都由两种相同的元素组成.在A和B中两种元素的原子个数比分别为1∶1和1∶2.将A和B在高温时煅烧,产物都是C(固体)和D(气体).由D最终可制得E(酸),E和另一种酸组成混合酸,常用于制取有机炸药.E的稀溶液和A反应时,生成G(气体)和F(溶液);G通入D的水溶液中,有浅黄色沉淀生成.在F中滴入溴水后,加入KOH溶液,有红褐色沉淀生成,该沉淀加热时又转变为C.
根据以上事实回答:
(1)A的化学式是________,B的化学式是________.
(2)写出下列反应的化学方程式:
①B煅烧生成C和D:________;
②G通入D的溶液中:________;
③在F中滴入溴水:________.
(3)写出A和E反应的离子方程式:________.
解析:
|
|
提示:
|
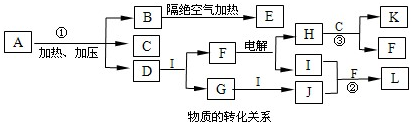
本题是元素化合物的综合推断题,涉及的知识点相当多,如FeS、FeS2的性质,SO2、H2SO4的性质,混合酸(H2SO4+HNO3)与甲苯、甘油、纤维素等反应生成炸药的性质、溴水的氧化性、Fe2+的还原性、Fe(OH)3的颜色及热分解的性质. 最后答题的落脚点是化学式、化学方程式、离子方程式等化学用语.所以要求学生基础知识要扎实,基本技能要熟练、准确.特别是后者,往往容易被忽视.应该说,尽管该题的综合性强、题目大,但由于突破点较明显、较多,所以并不属于难题. 突破点①:“固体A和B都由两种相同元素组成,原子个数比为1∶1和1∶2.”中学化学中涉及的固体二元化合物中,相同两种元素形成两种物质的有:Na2O和Na2O2,Cu2O和CuO,FeS和FeS2.再由后面的条件,容易确定是FeS和FeS2. 突破点②:“产生浅黄色沉淀……有红褐色沉淀.”浅黄色沉淀可以是硫单质或AgBr,红褐色沉淀只能是Fe(OH)3,而S或AgBr、Fe元素来自于A和B,即A和B中必含Fe元素,则另一元素应为非金属元素,且满足1∶1、1∶2,故A和B由S和Fe形成,分别为FeS和FeS2. 突破点③:“E和另一种酸组成混合酸,常用于制取有机炸药.”制有机炸药用硝酸做反应物,H2SO4做催化剂和脱水剂,所以E是H2SO4或HNO3,A和B含S或N.含氮的固体化合物不能满足1∶1和1∶2,故A和B应是含硫的化合物,从而推出是FeS和FeS2. 另外也可将题目中的文字叙述转化为如下框图,也是分析和解答此类题的重要手段.
|

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案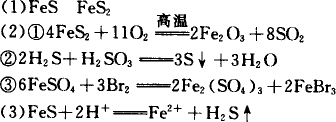


 NH4++NH2-
NH4++NH2-

