题目内容
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g)平衡时测得A的浓度为0.60mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.35mol/L.下列有关判断正确的是( )
| A、x+y<z |
| B、平衡向正反应方向移动 |
| C、B的转化率降低 |
| D、C的体积分数下降 |
考点:化学平衡的计算
专题:
分析:保持温度不变,将容器的体积扩大两倍,如平衡不移动,A的浓度为0.3mol/L,实际A的浓度变为0.35mol/L,说明平衡向生成A的方向移动,即向逆反应移动,据此结合选项解答.
解答:
解:保持温度不变,将容器的体积扩大两倍,如平衡不移动,A的浓度为0.3mol/L,实际A的浓度变为0.35mol/L,说明平衡向生成A的方向移动,即向逆反应移动,
A、平衡向逆反应移动,压强平衡向气体物质的量增大的方向移动,即x+y>z,故A错误;
B、由上述分析可知,平衡向逆反应移动,故B错误;
C、平衡向生成A的方向移动,即逆反应移动,B的转化率降低,故C正确;
D、平衡向逆反应移动,减小压强平衡向气体物质的量增大的方向移动,气体的物质的量增大,C物质的量减小,故C的体积分数下降,故D正确;
故选:CD.
A、平衡向逆反应移动,压强平衡向气体物质的量增大的方向移动,即x+y>z,故A错误;
B、由上述分析可知,平衡向逆反应移动,故B错误;
C、平衡向生成A的方向移动,即逆反应移动,B的转化率降低,故C正确;
D、平衡向逆反应移动,减小压强平衡向气体物质的量增大的方向移动,气体的物质的量增大,C物质的量减小,故C的体积分数下降,故D正确;
故选:CD.
点评:本题考查化学平衡移动,难度中等,利用假设法判断平衡移动方向是解题关键.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
常温下,下列有关醋酸的叙述中不正确的是( )
| A、pH=5.6的由CH3COOH与CH3COONa组成的混合溶液中:c(Na+)<c(CH3C00-) |
| B、将pH=a的醋酸稀释为pH=a+1的过程中,c(OH-)不断增大 |
| C、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14 |
| D、浓度均为o.1 mol-1的CH3COOH溶液和氨水等体积混合后:c(CH3COO-)+c(OH-)=c(H+)+c(NH4+) |
下列关于蒸馏操作的有关叙述不正确的是( )
| A、蒸馏操作时蒸馏烧瓶要垫上石棉网 |
| B、蒸馏操作使用的温度计的水银球应插入到液体内 |
| C、在蒸馏烧瓶内放入少量碎瓷片,目的是防止暴沸 |
| D、冷凝管进出水的方向是下口进水、上口出水 |
合金在生产及科研中具有广泛的应用.下列物质不属于合金的是( )
| A、黄铜 | B、水银 | C、不锈钢 | D、硬铝 |
如图是电解CuCl2溶液的装置,c、d为石墨电极,下列有关的判断正确的是( )
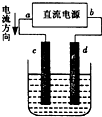

| A、电解过程中,d电极质量增加 |
| B、a为阳极、b为阴极 |
| C、a为负极、b为正极 |
| D、电解过程中,氯离子浓度基本不变 |