题目内容
有A、B、C、D四种无色溶液,它们分别是一定浓度的AlCl3溶液、盐酸、氨水、Na2SO4溶液中的一种.已知A、B溶液中水的电离程度相同,A、C溶液的pH相同.请回答下列问题:
(1)A是 ,B是 ,C是 ,D是 .
(2)写出足量B溶液与少量C溶液混合后发生反应的离子方程式: .
(3)A、B溶液等体积混合后,溶液中各离子浓度由大到小的顺序是: .
(1)A是
(2)写出足量B溶液与少量C溶液混合后发生反应的离子方程式:
(3)A、B溶液等体积混合后,溶液中各离子浓度由大到小的顺序是:
考点:几组未知物的检验
专题:物质检验鉴别题
分析:A、C溶液的pH相同,A、C为AlCl3溶液、盐酸,均显示酸性,A、B溶液中水的电离程度相同,A、B为盐酸、氨水,都对水的电离起到抑制作用,故A为盐酸,B为氨水溶液,C为AlCl3溶液,D为Na2SO4溶液,溶液的pH=7,以此解答该题.
解答:
解:A、C溶液的pH相同,A、C为AlCl3溶液、盐酸,均显示酸性,A、B溶液中水的电离程度相同,A、B为盐酸、氨水,都对水的电离起到抑制作用,故A为盐酸,B为氨水溶液,C为AlCl3溶液,D为Na2SO4溶液,
(1)A为盐酸,B为氨水溶液,C为AlCl3溶液,D为Na2SO4溶液,故答案为:盐酸;氨水;AlCl3溶液;Na2SO4溶液;
(2)足量氨水溶液与少量AlCl3溶液混合后,会生成氢氧化铝白色沉淀,发生反应的离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
(3)A为盐酸,B为氨水溶液,两溶液中水的电离程度相同,A、B溶液等体积混合后,生成氯化铵和水,溶液显示碱性,所以溶液中各离子浓度由大到小的顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+),故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+).
(1)A为盐酸,B为氨水溶液,C为AlCl3溶液,D为Na2SO4溶液,故答案为:盐酸;氨水;AlCl3溶液;Na2SO4溶液;
(2)足量氨水溶液与少量AlCl3溶液混合后,会生成氢氧化铝白色沉淀,发生反应的离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
(3)A为盐酸,B为氨水溶液,两溶液中水的电离程度相同,A、B溶液等体积混合后,生成氯化铵和水,溶液显示碱性,所以溶液中各离子浓度由大到小的顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+),故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+).
点评:本题考查无机物的推断,侧重于盐类水解的考查,注意把握盐类水解的规律和溶液酸碱性的判断,为解答该题的关键,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列描述正确的是( )
| A、摩尔是国际单位制中的一个基本物理量 |
| B、萃取操作时,可以选择有机萃取剂,且萃取剂的密度必须比水大 |
| C、当光束分别通过氢氧化铁胶体、氯化铁溶液时,都可以从侧面看见光亮的通路 |
| D、根据分散质粒子的直径大小,分散系可分为溶液、胶体和浊液 |
向某盐溶液中加入BaCl2溶液时,有不溶于稀HNO3的白色沉淀生成,而向该溶液中加入NaOH 溶液时有蓝色沉淀生成,则该盐的化学式为( )
| A、CuCO3 |
| B、Na2SO4 |
| C、CuSO4 |
| D、Cu(NO3)2 |
用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH;甲基橙变色范围为3.1一4.4).下列判断正确的是( )
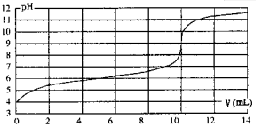

| A、HA的浓度为1×10-4mol?L-1 |
| B、实验时可选甲基橙作指示剂 |
| C、V=10mL,酸碱恰好中和 |
| D、pH=7时,溶液中c(Na+)>c(A-) |
有关甲醛(H2C=O)分子的说法正确的是( )
| A、C原子采取sp杂化 |
| B、甲醛分子为三角锥形结构 |
| C、C原子采取sp3杂化 |
| D、甲醛分子为平面三角形结构 |
茉莉醛具有浓郁的茉莉花香,其结构简式如图所示:关于茉莉醛的下列叙述错误的是( )
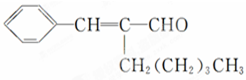
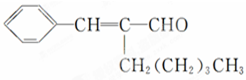
| A、在加热和催化剂作用下,能被氢气还原 |
| B、能被酸性高锰酸钾溶液氧化 |
| C、在一定条件下能与溴发生取代反应 |
| D、不能与氢溴酸发生加成反应 |
 现有一盛有常见固体物质M的试剂瓶,标签已破损(如图所示),请根据其性质回答下列问题:
现有一盛有常见固体物质M的试剂瓶,标签已破损(如图所示),请根据其性质回答下列问题: