题目内容
2.下列混合物完全燃烧生成CO2的量可能与燃烧等物质的量的乙烯生成CO2的量相等的是( )| A. | C2H6O和C3H8 | B. | CH4和C3H6 | C. | C3H6和C3H8 | D. | CH4和C2H2 |
分析 乙烯分子式为C2H4,物质的量相同时完全燃烧生成的二氧化碳的量相等,说明混合物中平均C原子数为2,据此对各选项进行判断.
解答 解:乙烯分子式为C2H4,混合物完全燃烧生成CO2的量与燃烧等物质的量的乙烯生成CO2的量相等,说明混合物的平均C原子数为2,
A.C2H6O和C3H8的平均碳原子数一定大于2,不满足条件,故A错误;
B.CH4和C3H6的物质的量之比为1:1时,平均碳原子数可以为2,满足条件,故B正确;
C.C3H6和C3H8的平均碳原子数为3,不满足条件,故C错误;
D.CH4和C2H2的平均碳原子数小于2,不满足条件,故D错误;
故选B.
点评 本题考查了有机物燃烧的计算,题目难度不大,明确题干信息的含义为解答关键,注意掌握平均值法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
13.有关物质结构的下列说法中正确的是( )
| A. | 石油裂解只破坏极性键 | |
| B. | 含极性键的共价化合物一定是电解质 | |
| C. | 氯化钠固体中的离子键在溶于水时被破坏 | |
| D. | HF的分子间作用力大于HCl,故HF比HCl稳定 |
17.向BaCl2溶液中通入SO2气体,溶液仍澄清;若将BaCl2溶液分盛两支试管,一支中加入H2O2,另一支中加入烧碱溶液,然后再通入SO2气体,结果两支试管都有白色沉淀生成.由此得出的下列结论合理的是( )
| A. | 氯化钡有两性 | |
| B. | 两支试管中产生的沉淀都是BaSO4 | |
| C. | 两支试管中的沉淀都是BaSO3 | |
| D. | H2SO3可被H2O2氧化为H2SO4,BaCl2与SO2不反应但能与SO${\;}_{3}^{2-}$反应 |
14.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是( )
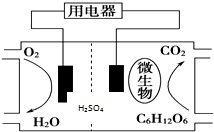

| A. | 葡萄糖在正极失去电子被氧化成CO2 | |
| B. | 微生物的作用是促进电路中电子的转移 | |
| C. | 质子通过交换膜从正极移向负极区 | |
| D. | 正极的电极反应式为O2+4H++4e-═2H2O |
12.某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1mol•L-1,某同学进行了如下实验:
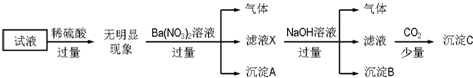
下列说法正确的是( )

下列说法正确的是( )
| A. | 原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42- | |
| B. | 无法确定原试液中是否含有K+ | |
| C. | 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+ | |
| D. | 无法确定沉淀C的成分 |