题目内容
下列条件下,可以大量共存的离子组是( )
| A、某无色溶液中:Na+、Cu2+、Cl-、MnO4- |
| B、含有大量Fe3+的溶液中:Na+、SO42-、K+、SCN- |
| C、含有大量NH4+的溶液中:Ba2+、K+、Cl-、OH- |
| D、在pH=1的溶液中:K+、Fe3+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.无色溶液中有颜色的离子不能大量共存;
B.与Fe3+反应的离子不能大量共存;
C.与NH4+反应的离子不能大量共存;
D.pH=1的溶液呈酸性.
B.与Fe3+反应的离子不能大量共存;
C.与NH4+反应的离子不能大量共存;
D.pH=1的溶液呈酸性.
解答:
解:A.Cu2+、MnO4-有颜色,不符合题目无色要求,故A错误;
B.SCN-与Fe3+反应而不能大量共存,故B错误;
C.OH-与NH4+反应而不能大量共存,故C错误;
D.pH=1的溶液呈酸性,酸性条件下离子之间不发生任何反应,可大量共存,故D正确.
故选D.
B.SCN-与Fe3+反应而不能大量共存,故B错误;
C.OH-与NH4+反应而不能大量共存,故C错误;
D.pH=1的溶液呈酸性,酸性条件下离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子的共存问题,为高频考点,侧重于学生的分析能力的考查,明确信息及信息的应用、熟悉离子之间的反应即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B、常温常压下,NO2和N2O4的混合物46g中约含有2NA个氧原子 |
| C、Na2O2与H2O反应生成1.12L O2(标准状况),反应中转移的电子数为6.02×1022 |
| D、标准状况下,80g SO3中含3NA个氧原子,体积约为22.4L |
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、常温下,将pH=2的盐酸和pH=12的氨水等体积混合:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、0.1mol?L-1 Na2CO3溶液:c(Na+)=c(HCO3-)+2c(CO32-)+2c(H2CO3) |
| C、0.1mol?L-1 NH4Cl溶液:c(NH4+)=c( Cl-) |
| D、向醋酸钠溶液加适量醋酸,得到的混合溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
下列解释实验事实的方程式不正确的是( )
| A、可用氯气进行自来水的杀菌消毒:Cl2+H2O═HCl+HClO |
| B、将“NO2球”浸泡在热水中,颜色变深:2NO2(g)═N2O4(g)△H<0 |
| C、在刻制印刷电路板时,用FeCl3溶液腐蚀铜箔:2Fe3++3Cu═2Fe+3Cu2+ |
| D、在KNO3和稀硫酸混合液中,铜片溶解:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
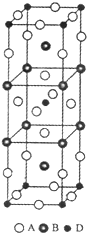 前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子总数相差为8;与B位于同一周期的C和D,它们的价电子层排布中未成对电子数分别为4和2,且原子序数相差为2.
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子总数相差为8;与B位于同一周期的C和D,它们的价电子层排布中未成对电子数分别为4和2,且原子序数相差为2.