题目内容
用氨碱生产NH4Cl和Na2CO3的主要过程是:在饱和NaCl溶液中,先通入足量的NH3气,然后再通入足量的CO2气体,析出NaHCO3晶体.主要反应有三步:
NH3+CO2+H2O→NH4HCO3
NH4HCO3+NaCl→NH4Cl+NaHCO3
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
若反应过程无损失,CO2可重复使用.
(1)通入NH3和CO2最适宜的体积比是(同温同压下)________;
(2)实际生产中,反应过程中需补充水和NaCl,补充水和NaCl的物质的量之比是________.
答案:
解析:
解析:
|
(1)2∶1;(2)1∶2 导解:将上述三个反应方程式进行叠加可得总反应式: 2NH3+CO2+H2O+2NaCl=2NH4Cl+Na2CO3,故有上述结论. |

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
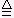 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O