题目内容
向8克二价金属的氧化物固体中加入稀硫酸,使其恰好完全溶解,已知所消耗的硫酸体积为100毫升,在所得溶液插入铂电极进行电解,通电一定时间后,在一个电极上收集到224毫升(标准状况)氧气,在另一个电极上得到1.28克该金属。
(1)根据计算确定金属氧化物的名称。
(2)计算通电后硫酸溶液的物质量浓度(溶液体积按100毫升计算)。
【答案】
(1)氧化铜(2)硫酸溶液的浓度为0.2mol/L
【解析】
试题分析:(1)生成氧气的物质的量是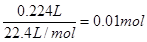
所以转移电子的物质的量是0.01mol×4=0.04mol
则根据M2++2e-=M可知
金属M的物质的量是0.02mol
所以M的相对原子质量是1.28÷0.02=64
因此M是金属铜
则该金属氧化物的名称是氧化铜
(2)根据铜原子守恒可知
硫酸铜的物质的量是0.02mol
则稀硫酸的物质的量也是0.02mol
所以稀硫酸的难度是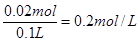
考点:考查电解池的有关计算
点评:本题是基础性试题的考查,难度不大。主要是巩固学生对电解原理的理解掌握程度,以及灵活运用知识的能力,同时也有利于培养学生的规范答题能力,提高学习效率。

练习册系列答案
相关题目