题目内容
14.可用分液漏斗分离的一组混合物是( )| A. | 硝基苯和酒精 | B. | 溴苯和溴 | C. | 甲苯和水 | D. | 硝基苯和己烷 |
分析 能用分液漏斗分离的物质必须是两种相互不溶的液体,一般的来说:有机溶质易溶于有机溶剂,无机溶质易溶于无机溶剂.
解答 解:题中硝基苯和酒精、溴苯和溴、硝基苯和己烷可互溶,不能用分液的方法分离,可用蒸馏的方法分离,而甲苯和水互不相溶,可用分液的方法分离,
故选C.
点评 本题考查物质的分离,为高频考点,侧重于学生的分析、实验能力的考查,题目难度不大,本题注意把握常见混合物的分离原理、方法以及操作的注意事项等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.金刚石是典型的原子晶体,下列关于金刚石的说法中错误的是( )
| A. | 晶体中不存在独立的“分子” | |
| B. | 含有1 mol C的金刚石中,形成的共价键有2 mol | |
| C. | 是自然界中硬度最大的物质 | |
| D. | 化学性质稳定,即使在高温下也不会与氧气发生反应 |
9.下列有关元素的性质及其递变规律正确的是( )
| A. | 同周期金属元素的化合价越高,其原子失电子能力越强 | |
| B. | 同主族元素的简单阴离子还原性越强,其氢化物越稳定 | |
| C. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| D. | IA族与ⅦA族元素间能形成离子化合物或共价化合物 |
19.在25℃时,在水中通入氯化氢气体,当溶液的pH等于3时,此时由水本身电离出的c(H+)是(mol•L-1)( )
| A. | 10-3 | B. | 10-7 | C. | 10-11 | D. | 10-14 |
3.下列有关实验说法中,正确的是( )
| A. | 用浓硝酸做试剂比较铁和铜的金属活动性 | |
| B. | 使用干燥洁净玻璃棒将氯水滴在干燥pH试纸上,测定氯水的pH | |
| C. | 欲检验Br-的存在,可在溶液中先加入氯水、再加入CCl4,振荡、静置,观察下层溶液显橙红色 | |
| D. | 氢氧化铁胶体在直流电场中,一段时间阴极附近红褐色加深,说明胶体带正电荷 |
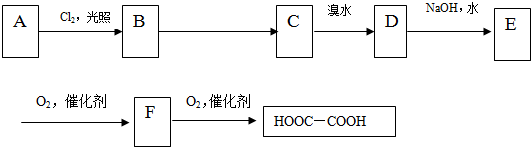
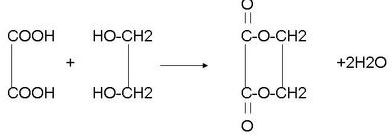 .
. ,含有离子键和非极性共价键的化合物的电子式为
,含有离子键和非极性共价键的化合物的电子式为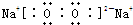 ;含有极性共价键和非极性共价键的化合物的电子式为
;含有极性共价键和非极性共价键的化合物的电子式为 .
. .
.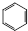 +HNO3$\stackrel{催化剂}{→}$
+HNO3$\stackrel{催化剂}{→}$ +H2O,反应类型取代反应
+H2O,反应类型取代反应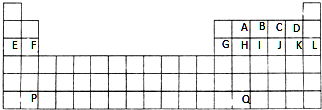
 .
.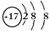 .
.