题目内容
16.下列有关性质的比较,不能用元素周期律解释的是( )| A. | 氧化性:Fe3+>Cu2+ | B. | 还原性:Br->Cl- | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 酸性:H2SO4>H3PO4 |
分析 A.金属阳离子的氧化性强弱与其得电子难易程度有关;
B.同一主族元素,元素的非金属性越强,其简单阴离子的还原性越弱;
C.同一周期元素,元素的金属性越强,其最高价氧化物的水化物碱性越强;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强.
解答 解:A.铁离子、铜离子的氧化性强弱与其得电子难易程度有关,与元素周期律无关,故A选;
B.同一主族元素,元素的非金属性越强,其简单阴离子的还原性越弱,非金属性Cl>Br,所以还原性:Br->Cl-,故B不选;
C.同一周期元素,元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性Na>Mg,所以碱性:NaOH>Mg(OH)2,故C不选;
D.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S>P,所以酸性:H2SO4>H3PO4,故D不选;
故选A.
点评 本题考查元素周期律,为高频考点,明确同一周期、同一主族元素原子结构与元素性质关系是解本题关键,熟练掌握元素周期律,题目难度不大.

练习册系列答案
相关题目
6.2012年某媒体报道了“皮革奶”事件,不法厂商将皮革下脚料水解后掺入奶粉以提高奶粉中蛋白质的含量.下列说法不正确的是( )
| A. | 动物皮革的主要成分是蛋白质 | |
| B. | 天然蛋白质水解的最终产物是α氨基酸 | |
| C. | 皮革鞣制过程中使用的浓HNO3会使蛋白质盐析 | |
| D. | “皮革奶”灼烧时有烧焦羽毛的气味 |
7.已知${\;}_{17}^{35}$Cl的相对原子质量为34.969,下列相关说法正确的是( )
| A. | 氯元素的近似相对原子质量为35 | B. | 氯元素的某种同位素的质量数为35 | ||
| C. | 氯元素的中子数为18 | D. | 氯原子的质量为34.969 |
5.肉桂酸异戊酯是一种香料,其结构简式如图.下列有关肉桂酸异戊酯的叙述正确的是( )
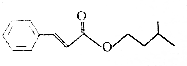

| A. | 不能使溴的四氯化碳溶液褪色 | |
| B. | 能与新制的Cu(OH)2共热生成红色沉淀 | |
| C. | 能与FeCl3溶液反应显紫色 | |
| D. | 能与热的浓硝酸和浓硫酸混合液反应 |
2.在一固定体积的密闭容器中,充入2mol CO2和1mol H2发生如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$.
(2)若反应在830℃下达到平衡,则CO2气体的转化率为$\frac{1}{3}$.
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度升高(填“升高”、“降低”或“不能确定”).
(4)在830℃达平衡后在其容器中分别仅充入1mol CO2 和1molCO后,该反应的v正小于 v逆((填“大于”“小于”“等于”),平衡向逆方向移动.
| t(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$.
(2)若反应在830℃下达到平衡,则CO2气体的转化率为$\frac{1}{3}$.
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度升高(填“升高”、“降低”或“不能确定”).
(4)在830℃达平衡后在其容器中分别仅充入1mol CO2 和1molCO后,该反应的v正小于 v逆((填“大于”“小于”“等于”),平衡向逆方向移动.
 的路线:
的路线: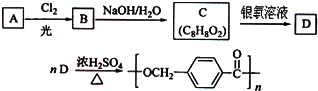
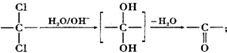
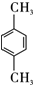 .
. ,该反应过程中生成的不稳定中间体的结构简式应是
,该反应过程中生成的不稳定中间体的结构简式应是 .
.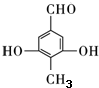 .
.