题目内容
15.下列装置或操作能达到实验目的是( )| A. | 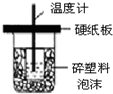 如图装置用于中和热的测定 | |
| B. | 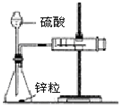 如图装置用于测定氢气的反应速率(单位mL/s) | |
| C. | 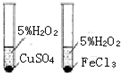 如图装置用于研究催化剂Cu2+和Fe3+对反应速率的影响 | |
| D. | 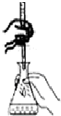 如图装置用于已知浓度的高锰酸钾溶液测定未知浓度的草酸溶液 |
分析 A.缺少环形玻璃棒;
B.气体从长颈漏斗逸出;
C.研究催化剂Cu2+和Fe3+对反应速率的影响,应用等浓度的氯化铜、氯化铁溶液;
D.高锰酸钾具有强氧化性,放在酸式滴定管中.
解答 解:A.缺少环形玻璃搅拌棒,故A错误;
B.气体从长颈漏斗逸出,无法收集气体,且缺少秒表,故B错误;
C.研究催化剂Cu2+和Fe3+对反应速率的影响,应用等浓度的氯化铜、氯化铁溶液,不能用固体,故C错误;
D.高锰酸钾具有强氧化性,放在酸式滴定管中,可完成实验,故D正确.
故选D.
点评 本题考查较为综合,涉及中和热的测定、反应速率的测定、反应速率的影响以及滴定等操作,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握实验的严密性以及和可行性的评价,难度不大.

练习册系列答案
相关题目
5.某物质灼烧时,焰色反应为黄色,则下列判断不正确的是( )
| A. | 该物质可能是钠的化合物 | B. | 该物质一定含钠元素 | ||
| C. | 不能确定该物质中是否含有钾元素 | D. | 该物质一定是金属钠 |
6.部分弱酸的电离平衡常数如下表:
下列选项错误的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.77×10-4 | 4.9×10-16 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 2CN-+H2O+CO2═2HCN+CO32- | |
| B. | 2HCOOH+CO32-═2HCOO-+H2O+CO2↑ | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 | |
| D. | HCOOH+CN-═HCOO-+HCN |
3.下列实验操作及现象结论描述不准确的是( )
| A. | 向沸水中滴加饱和氯化铁溶液制备胶体,用可见光束照射,产生丁达尔效应 | |
| B. | 常温下,向0.10mol•L-1NaHCO3溶液,滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出,说明加入CaCl2促进了HCO3-的水解 | |
| C. | 利用以下实验器材(规格数量不限):烧杯、量筒、环形玻璃搅拌棒、纸条、硬纸板、温度计能完成中和反应反应热的测定 | |
| D. | 向浓度均为0.1mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,先出现蓝色沉淀,因为KSP[Mg(OH)2]>KSP[Cu(OH)2] |
7.工业上利用氢气在氯气中燃烧,所得产物再溶于水的方法制得盐酸,流程复杂且造成能量浪费.有人设想利用原电池原理直接制盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是( )
| A. | 通入氢气的电极为原电池的正极 | |
| B. | 两极材料都用石墨,用稀盐酸做电解质溶液 | |
| C. | 电解质溶液中的阳离子向通氯气的电极移动 | |
| D. | 通氯气的电极反应式为Cl2+2e-═2Cl- |
4.分类思想是中学化学的核心思想,分类均有一定标准.下列有关说法正确的是 ( )
| A. | SiO2、NaHCO3均可能与强酸、强碱反应,都为两性物质 | |
| B. | Na2CO3、CH3COOH、Cu2(OH)2CO3均含有碳元素,都是有机化合物 | |
| C. | BaCO3、BaSO3、BaSO4均难溶于水,均属于难溶电解质 | |
| D. | HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
17.第一次用无机物制得有机物尿素,开辟人工合成有机物先河的科学家是( )
| A. | 德国的维勒 | B. | 瑞典的贝采里乌斯 | ||
| C. | 德国的李比希 | D. | 匈牙利的海维西 |
 .
. .
.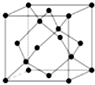 A、B、C、D、E、F为原子序数依次增大的六种元素,A的一种同位素可用于考古测定生物的死亡年代,C原子的最外层电子数是次外层的3倍,D与B同主族;E的原子序数是A、B之和的2倍;F的原子序数为29.回答下列问题:
A、B、C、D、E、F为原子序数依次增大的六种元素,A的一种同位素可用于考古测定生物的死亡年代,C原子的最外层电子数是次外层的3倍,D与B同主族;E的原子序数是A、B之和的2倍;F的原子序数为29.回答下列问题: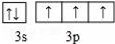 .
.