题目内容
实验室常用浓H2SO4与硝酸钠反应制HNO3,其方程式为:NaNO3+H2SO4
NaHSO4+HNO3↑,制取HNO3时,如图所列装置中最适合的是( )
| 微热 |
A、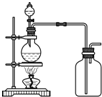 |
B、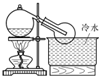 |
C、 |
D、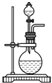 |
考点:硝酸的化学性质
专题:氮族元素
分析:根据化学反应原理,硝酸的制取原理是:固体和液体微热制取,难挥发性的酸来制取挥发性的酸,据此选择装置.
解答:
解:硝酸的制取原理是:固体和液体微热制取,故D错误,该反应符合难挥发性的酸来制取挥发性的酸,硝酸易挥发,不能用排空气法收集,故A、C错误;所以硝酸的挥发性注定了选择的收集方法是B装置所示.
故选B.
故选B.
点评:本题涉及气体的制取原理知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示),下列有关说法正确的是( )


| A、第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3、NaOH、BaCl2和盐酸 |
| B、第②步中结晶出的MgCl2?6H2O可在空气中受热分解制无水MgCl2 |
| C、在第③④⑤步中溴元素均被氧化 |
| D、由海水提取的金属镁能与金属铝、氢氧化钠溶液在一定条件下形成原电池,金属镁作该原电池正极 |
下列推断正确的是( )
| A、NH3、HCl的水溶液都能导电,但NH3不是电解质 |
| B、Na2O、Na2O2组成元素相同,与CO2反应产物也相同 |
| C、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D、新制氯水和SO2都具有漂白性,都能使紫色石蕊试液褪色 |
下列物质可以用来鉴别乙醇、乙酸、乙酸乙酯的试剂是( )
| A、稀硫酸 | B、NaOH溶液 |
| C、碳酸钠溶液 | D、酚酞溶液 |
下列各组离子在指定溶液中一定能大量共存的是( )
| A、能使甲基橙呈红色的溶液:Ba2+、Al3+、NO3-、Cl- |
| B、由水电离出的c(H+)=1×10-11 mol?L-1溶液:Na+、Mg2+、Cl-、NO3- |
| C、0.2 mol?L-1的NaNO3溶液:H+、Fe2+、SO42-、Cl- |
| D、与Fe反应生成H2的溶液:NH4+、K+、SO42-、CO32- |
设NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A、室温下,1mol SO3含有的分子数为NA个 |
| B、0.1molAl3+离子含有核外电子数为NA个 |
| C、1molCl2与1mol Fe反应,转移电子为3 NA个 |
| D、标准状况下2.24L己烷含有分子数目为0.1 NA个 |

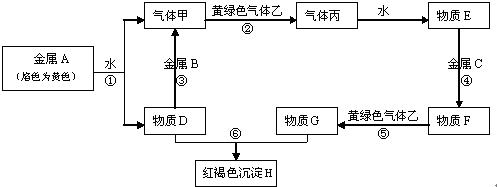
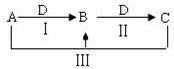 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).