题目内容
Ⅱ.煤是化石燃料.煤燃烧的反应热可通过以下两个途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳,然后是使得到的氢气和一氧化碳在充足的空气中燃烧.
这两个过程的化学方程式为:
a.C(s)+O2(g)=CO2(g)△H=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g)△H=E2 ②
H2(g)+
O2(g)=H2O(g)△H=E3 ③
CO(g)+
O2(g)=CO2(g)△H=E4 ④
请回答:
(1)上述四个热化学方程式中哪个反应△H>0? (填序号)
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是 .
A.a比b多 B. a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为 .
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳,然后是使得到的氢气和一氧化碳在充足的空气中燃烧.
这两个过程的化学方程式为:
a.C(s)+O2(g)=CO2(g)△H=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g)△H=E2 ②
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
请回答:
(1)上述四个热化学方程式中哪个反应△H>0?
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B. a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为
考点:用盖斯定律进行有关反应热的计算,反应热和焓变
专题:
分析:(1)燃烧反应均为放热反应,C与水蒸气的反应为吸热反应;
(2)根据盖斯定律可知,反应一步完成或分步完成,其热效应相同;
(3)利用盖斯定律来分析.
(2)根据盖斯定律可知,反应一步完成或分步完成,其热效应相同;
(3)利用盖斯定律来分析.
解答:
解:(2)因为燃烧反应均为放热反应,①③④为燃烧反应,属于放热反应,△H<0,②为吸热反应,△H>0;
故答案为:②;
(3)由盖斯定律可知,反应一步完成或分步完成,其热效应相同,则等质量的煤分别通过以上两条不同的途径产生的可利用的总能量相同,
故答案为:C;
(4)由盖斯定律可知,反应一步完成或分步完成,其热效应相同,所以①=②+③+④,则能量为E1=E2+E3+E4,
故答案为:E1=E2+E3+E4.
故答案为:②;
(3)由盖斯定律可知,反应一步完成或分步完成,其热效应相同,则等质量的煤分别通过以上两条不同的途径产生的可利用的总能量相同,
故答案为:C;
(4)由盖斯定律可知,反应一步完成或分步完成,其热效应相同,所以①=②+③+④,则能量为E1=E2+E3+E4,
故答案为:E1=E2+E3+E4.
点评:本题考查化学反应中的能量变化及利用盖斯定律确定反应及其能量的关系,注重基础知识的考查,题目较简单.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
下列由极性键构成的非极性分子是( )
| A、N2 |
| B、HF |
| C、NH3 |
| D、CO2 |
下列离子方程式正确的是( )
A、甘氨酸(α-氨基乙酸)与氢氧化钠溶液反应: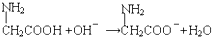 | ||
| B、高级脂肪酸与氢氧化钠溶液反应:H++OH-=H2O | ||
| C、苯酚钠溶液中通入少量CO2:2C6H5O-+H2O+CO2→2C6H5OH+CO32- | ||
D、乙醛与银氨溶液的反应:CH3CHO+2[Ag(NH3)2]++2OH-
|
关于物质分类正确的组合是( )
| 分类 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | CaF2 | CO | Al2O3 |
| D | KOH | HNO3 | CaCO3 | CaO | SO3 |
| A、A | B、B | C、C | D、D |
在由水电离产生的H+浓度为1×10-11 mol/L的溶液中,一定能大量共存的离子组是( )
①K+、Cl-、NO3-、S2-; ②K+、Al3+、I-、SO42-; ③Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-.
①K+、Cl-、NO3-、S2-; ②K+、Al3+、I-、SO42-; ③Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-.
| A、①③ | B、②⑤ | C、③④ | D、③⑤ |
能大量共存于同一溶液中的离子组是( )
| A、H+、K+、HCO3- |
| B、Ag+、NO3-、Cl- |
| C、CO32-、Na+、Ba2+ |
| D、NO3-、Cl-、H+ |
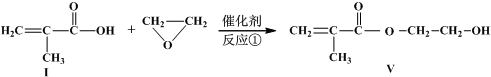
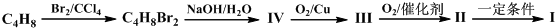
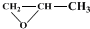 发生类似反应①的反应,试写出其中一种产物的结构式:
发生类似反应①的反应,试写出其中一种产物的结构式: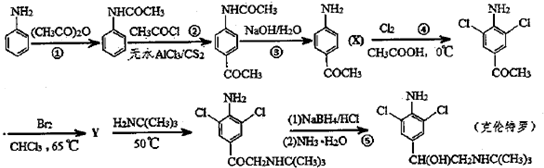
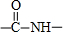 且能发生银镜反应的X的同分异构体有
且能发生银镜反应的X的同分异构体有