题目内容
实验室中用二氧化锰固体和浓盐酸制备氯气,应选用的下列气体发生装置是( )
A、 |
B、 |
C、 |
D、 |
考点:常见气体制备原理及装置选择
专题:化学实验基本操作
分析:二氧化锰固体和浓盐酸在加热条件下生成氯气,据此判断.
解答:
解:二氧化锰固体和浓盐酸在加热条件下生成氯气,该反应为固液反应,需要加热,所以符合实验要求的装置是D;
故选D.
故选D.
点评:本题考查了实验室制备氯气,主要考查了装置的选择,根据反应物的状态和反应条件选择,题目难度不大.

练习册系列答案
相关题目
 甲烷分子中的4个氢原子全部被苯基取代,所得物质的分子结构如图所示,对该物质的描述不正确的是( )
甲烷分子中的4个氢原子全部被苯基取代,所得物质的分子结构如图所示,对该物质的描述不正确的是( )| A、其分子式为C25H20 |
| B、分子内的所有碳原子不可能共平面 |
| C、该物质光照下可和氯气发生反应 |
| D、该物质在FeBr3催化下可和液溴发生反应 |
已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)△H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l)△H4;
则△H四者的关系中正确的是( )
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)△H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l)△H4;
则△H四者的关系中正确的是( )
| A、△H1>△H2>△H3>△H4 |
| B、△H4>△H2>△H3>△H1 |
| C、△H3>△H4>△H1>△H2 |
| D、△H4>△H3>△H2>△H1 |
有机物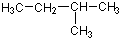 的名称是( )
的名称是( )
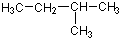 的名称是( )
的名称是( )| A、2-甲基丁烷 |
| B、3-甲基丁烷 |
| C、2-乙基丙烷 |
| D、1,1-二甲基丙烷 |
6克含杂质的Na2SO3样品与足量盐酸反应,可生成1.12升气体(S、T、P),气体质量为3克,该样品的组成可能是( )
| A、Na2SO3,Na2CO3 |
| B、Na2SO3,NaHCO3 |
| C、Na2SO3,NaHCO3,Na2CO3 |
| D、Na2SO3,MgCO3,NaHCO3 |
下列各组中的两种有机化合物,属于同系物的是( )
| A、2-甲基丁烷和丁烷 |
| B、新戊烷和2,2-二甲基丙烷 |
| C、间二甲苯和乙苯 |
| D、1-己烯和环己烷 |
下列说法正确的是( )
| A、凡是卤代烃一定能够发生消去反应 |
| B、卤代烃在碱性溶液中的水解反应属于取代反应 |
| C、苯酚显弱酸性,其溶液可使石蕊试液变红色 |
| D、正丁烷的沸点比异丁烷低 |
下列离子方程式中,正确的是( )
| A、在氯化铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
| B、在硝酸银溶液中滴入氯化钠溶液:Ag++Cl-=AgCl↓ |
| C、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
下列叙述正确的是( )
| A、强酸溶液中的氢离子浓度一定大于弱酸溶液中的氢离子浓度 |
| B、NaOH溶液的导电性一定比氨水的导电性强 |
| C、不溶性盐都是弱电解质,可溶性酸都是强电解质 |
| D、二氧化硫和乙醇均属共价化合物,是非电解质 |