题目内容
下列各组离子反应可以用H++OH-=H2O表示的有( )
| A、Cu(OH)2和HNO3 |
| B、Ba(OH)2与H2SO4 |
| C、CO2和NaOH溶液 |
| D、KHSO4和NaOH |
考点:离子方程式的书写
专题:离子反应专题
分析:离子方程式可表示一类反应,如离子方程式H++OH-═H2O表示强酸和可溶性强碱反应生成可溶性的盐和水的一类反应,据此对各选项进行判断.
解答:
解:A.Cu(OH)2为难溶物,离子方程式中不能拆开,Cu(OH)2与硝酸的反应不能用H++OH-=H2O表示,故A错误;
B.氢氧化钡与硫酸反应生成硫酸钡和水,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用H++OH-=H2O表示,故B错误;
C.二氧化碳为气体,离子方程式中需要保留化学式,不能用离子方程式H++OH-=H2O表示,故C错误;
D.硫酸氢钾为强电解质,溶液中完全电离出氢离子,硫酸氢钾与氢氧化钠反应生成可溶性盐和水,反应的离子方程式为:H++OH-=H2O,故D正确;
故选D.
B.氢氧化钡与硫酸反应生成硫酸钡和水,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用H++OH-=H2O表示,故B错误;
C.二氧化碳为气体,离子方程式中需要保留化学式,不能用离子方程式H++OH-=H2O表示,故C错误;
D.硫酸氢钾为强电解质,溶液中完全电离出氢离子,硫酸氢钾与氢氧化钠反应生成可溶性盐和水,反应的离子方程式为:H++OH-=H2O,故D正确;
故选D.
点评:本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式表示的意义为解答关键,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
邻苯二甲醛(X)在碱性条件下发生歧化(即自身氧化还原)反应,再经酸化得到化合物Y.Y可在浓硫酸存在的条件下生成含五元环的化合物Z.则下列说法正确的是( )
| A、邻二甲苯不可用作生产X的原料 |
| B、Y可发生银镜反应 |
| C、Y可与FeCl3发生显色反应 |
| D、Z与X的相对分子质量相等 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- | ||||
B、用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O
| ||||
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | ||||
| D、钢铁发生电化学腐蚀的负极反应式:Fe-2e-=Fe2+ |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、7.8 g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA | ||
B、标准状况下,a L的氧气和氮气的混合物含有的分子数为(
| ||
| C、60 g SiO2晶体中含有2NA个Si-O键 | ||
| D、标准状况下,11.2 L乙醇完全燃烧产生的CO2的分子数为0.5NA |
在无色强酸性溶液中,下列各组离子一定能大量共存的是( )
| A、Na+、K+、Cl-、SO42? |
| B、Cu2+、K+、SO42-、NO3- |
| C、K+、NH4+、SO42-、CO32? |
| D、Ba2+、Na+、Cl-、SO42- |
下列事实与胶体性质无关的是( )
| A、在豆浆里加入盐卤做豆腐 |
| B、在河流入海处易形成沙洲 |
| C、“尿毒症”患者做血液透析治疗 |
| D、三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
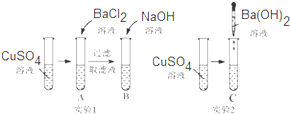
 (1)现有以下物质①NaOH溶液 ②干冰 ③稀硫酸 ④铜 ⑤醋酸 ⑥BaSO4固体 ⑦蔗糖 ⑧食盐晶体 ⑨酒精 ⑩熔融的KNO3,其中属于电解质的是:
(1)现有以下物质①NaOH溶液 ②干冰 ③稀硫酸 ④铜 ⑤醋酸 ⑥BaSO4固体 ⑦蔗糖 ⑧食盐晶体 ⑨酒精 ⑩熔融的KNO3,其中属于电解质的是: