题目内容
3.下列关于晶体的叙述中,不正确的是…( )| A. | 金刚石网状结构中,由共价键形成的碳原子环其中最小环有6个碳原子 | |
| B. | 在氯化钠的晶体中,每个Na+或Cl-的周围都紧邻6个Cl-或Na+ | |
| C. | 在氯化铯晶体中,每个Cs+周围都紧邻8个Cl-,每个Cl-周围也紧邻8个Cs+ | |
| D. | 在干冰的晶体中,每个CO2分子周围都紧邻4个CO2分子 |
分析 A.金刚石的结构中,每个碳原子能形成4个共价键,根据教材图片确定由共价键形成的最小碳环上的碳原子个数;
B、氯化钠晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(Na+);
C.根据CsCl晶胞图 确定;
确定;
D.干冰是分子晶体,CO2分子位于立方体的顶点和面心上,以顶点上的CO2分子为例,与它距离最近的CO2分子分布在与该顶点相连的12个面的面心上.
解答 解:A.金刚石结构中,每个碳原子能形成4个共价键,由共价键形成的最小碳环上有6个碳原子,故A正确;
B、已知氯化钠的晶胞图为 ,则氯化钠晶胞中,钠离子的配位数为6,即每个Na+或Cl-的周围都紧邻6个Cl-或Na+,故B正确;
,则氯化钠晶胞中,钠离子的配位数为6,即每个Na+或Cl-的周围都紧邻6个Cl-或Na+,故B正确;
C.已知晶胞图为 ,在CsCl晶体中每个Cs+周围都紧邻8个Cl-,每个Cs+等距离紧邻的有8个Cs+,故C正确;
,在CsCl晶体中每个Cs+周围都紧邻8个Cl-,每个Cs+等距离紧邻的有8个Cs+,故C正确;
D.从二氧化碳的基本结构可以知道,若以其中一个为中心,与其紧邻的二氧化碳分子有3×8÷2=12个,且相距均为边长的二分之根下二倍,故D错误,
故选:D.
点评 本题考查晶体结构,明确晶胞结构是解本题关键,难点是配位数的计算,难度中等.

练习册系列答案
相关题目
14.归纳整理是科学学习的重要方法之一.氧族元素的部分性质归纳整理如下:
请根据上表数据以及数据变化趋势,回答下列问题:
(1)硒的熔点范围可能是:113℃~450℃
(2)碲(Te)可能的化合价有:-2,+4,+6
(3)硒(Se)的原子半径可能在0.102~0.136之间.
(4)从单质与氢化合的难易程度可以推测出,O、S、Se、Te的非金属性逐渐减弱(增强、减弱).
元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点/℃ | -218,4 | 113 | ? | 450 |
| 单质沸点/℃ | -183 | 444.6 | 685 | 989 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | ? |
| 原子半径/nm | 0.074 | 0.102 | ? | 0.136 |
| 单质与氢化合的难易程度 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接 |
(1)硒的熔点范围可能是:113℃~450℃
(2)碲(Te)可能的化合价有:-2,+4,+6
(3)硒(Se)的原子半径可能在0.102~0.136之间.
(4)从单质与氢化合的难易程度可以推测出,O、S、Se、Te的非金属性逐渐减弱(增强、减弱).
11.用已知浓度的NaOH滴定未知浓度的盐酸,下列操作(其他操作正确) 会造成测定结果偏高的是( )
| A. | 滴定终点读数时俯视读数 | |
| B. | 锥形瓶洗净后未干燥 | |
| C. | 碱式滴定管滴定前尖嘴部分有气泡,滴定后气泡消失 | |
| D. | 酸式滴定管使用前,水洗后未用待测盐酸润洗 |
18.在盛有稀H2SO4的烧杯中放入用导线连接锌片和铜片,下列叙述正确的是( )
| A. | 正极附近的 SO42-离子浓度逐渐增大 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 溶液的pH逐渐变小 | |
| D. | 铜片上有H2逸出 |
8.电解原理在化学工业中有着广泛的应用.图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.则下列说法不正确的是( )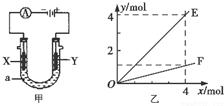

| A. | 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 | |
| B. | 按图甲装置用惰性电极电解AgN03溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 | |
| C. | 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol | |
| D. | 若X、Y为铂电极.a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol•L-1 |
15.下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( )
| A. | CH3CH(CH3)2 | B. | CH3CH2CH2CH3 | C. | (CH3)2CHCH2CH3 | D. | CH3C(CH3)3 |
12.下列说法正确的是( )
| A. | Na2O2中只含有离子键 | B. | HCl分子中含有离子键 | ||
| C. | 12C、13C、14C是碳的三种核素 | D. | 16O、17O、18O含有相同的中子数 |

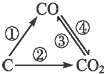 随着世界工业经济发展、人口剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.图为C及其氧化物的变化关系图,若变化①是置换反应,图中变化过程哪些是吸热反应①③(填序号).
随着世界工业经济发展、人口剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.图为C及其氧化物的变化关系图,若变化①是置换反应,图中变化过程哪些是吸热反应①③(填序号).