题目内容
16.下列化学反应的离子方程式表示正确的是( )| A. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| B. | 向Ca(HCO3)2溶液中滴加少量Ba(OH)2溶液:Ca2++2HCO3-+Ba2++2OH-═CaCO3↓+BaCO3↓+2H2O | |
| C. | 向NaHSO4溶液中加入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | Fe(OH)2沉淀中滴加稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
分析 A.二氧化碳过量,反应生成硅酸沉淀和碳酸氢根离子;
B.二者反应生成碳酸钙、碳酸钡和水;
C.向NaHSO4溶液中加入Ba(OH)2溶液至中性,反应生成硫酸钡、硫酸钠和水;
D.硝酸根离子具有强的氧化性,能够氧化二价铁离子生成三价铁离子;
解答 解:A.向Na2SiO3溶液中通入过量CO2,离子方程式:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-,故A错误;
B.向Ca(HCO3)2溶液中滴加少量Ba(OH)2溶液,离子方程式:Ca2++2HCO3-+Ba2++2OH-═CaCO3↓+BaCO3↓+2H2O,故B正确;
C.向NaHSO4溶液中加入Ba(OH)2溶液至中性,反应生成硫酸钡、硫酸钠和水,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D.氢氧化亚铁和稀硝酸发生氧化还原反应生成铁离子、NO和水,离子方程式为3Fe(OH)2+NO3-+10H+=3Fe3++NO↑+8H2O,故D错误;
故选:B.
点评 本题考查离子方程式正误判断,涉及氧化还原反应、离子反应,注意反应物的量对产物的影响,注意离子反应遵循客观事实,题目难度不大.

练习册系列答案
相关题目
6.W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( )

| A. | W、Y、X三种元素的原子半径依次减小 | |
| B. | Z元素的气态氢化物的热稳定性比Y的高 | |
| C. | W元素与氢元素可能会形成W2H6 | |
| D. | Y元素的单质能从NaZ溶液中置换出Z元素的单质 |
7.下列操作中仪器使用不正确的是( )
| A. | 容量瓶未经干燥不能用来配制溶液 | |
| B. | 用铁坩埚灼烧烧碱 | |
| C. | 中和热的测定实验中用环形玻璃棒搅拌 | |
| D. | 加热蒸发皿时不用石棉网 |
11.某无色混合气体可能含有CO2、H2、CO和H2O(气)中的一种或几种,依次进行以下处理(假设每次处理均反应完全):①通过盛有硅胶的干燥管时,气体体积不变;②通过炽热的氧化铜时,固体变为红色;③通过白色CuSO4粉末时,粉末变蓝色;④通过澄清石灰水时,溶液变浑浊.则原混合气体的成分不可能是( )
| A. | H2和CO | B. | CO2、H2和CO | C. | H2O | D. | H2和CO2 |
1.下列说法不正确的是( )
| A. | 分子组成相差一个或若干个CH2原子团的有机物是同系物 | |
| B. | 乙酸的官能团是羧基,乙醇的官能团是羟基 | |
| C. | 乙烯的产量通常用来衡量一个国家的石油化工发展水平 | |
| D. | 淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |
5.下列各组中的离子,能在无色溶液中大量共存的是( )
| A. | H+、K+、CO32-、SO42- | B. | Fe3+、Na+、NO3-、SO42- | ||
| C. | Mg2+、Ba2+、OH-、NO3- | D. | K+、Mg2+、NO3-、Cl- |
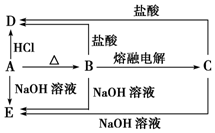 A、B、C、D、E五种物质均含有某种常见金属元素,它们的转化关系如图所示,其中B为白色难溶固体,E易溶于水.
A、B、C、D、E五种物质均含有某种常见金属元素,它们的转化关系如图所示,其中B为白色难溶固体,E易溶于水.