题目内容
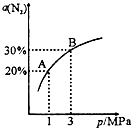 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α%)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α%)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A、将1.0mol氮气和3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ |
| B、平衡状态由A变到B时,平衡常数K(A)<K(B) |
| C、上述反应在达到平衡后,增大压强,H2的转化率提高 |
| D、升高温度,平衡向逆反应方向移动 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:
分析:A、可逆反应反应物不能完全转化,结合热化学方程式的含义解答;
B、平衡常数只受温度影响,与压强无关;
C、增大压强平衡向体积减小的方向移动;
D、升温平衡向吸热的逆方向移动.
B、平衡常数只受温度影响,与压强无关;
C、增大压强平衡向体积减小的方向移动;
D、升温平衡向吸热的逆方向移动.
解答:
解:A、热化学方程式N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol表示1mol氮气(g)以3mol氢气(g)反应生成2mol氨气(g),放出的热量为92.4kJ,由于可逆反应反应物不能完全转化,1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量小于92.4kJ,故A错误;
B、平衡常数只受温度影响,与压强无关,增大压强平衡常数不变,故平衡常数k(A)=k(B),故B错误;
C、增大压强平衡向体积减小的方向移动,即向正反应移动,H2的转化率提高,故C正确;
D、升温平衡向吸热的逆方向移动,故D正确.
故选CD.
B、平衡常数只受温度影响,与压强无关,增大压强平衡常数不变,故平衡常数k(A)=k(B),故B错误;
C、增大压强平衡向体积减小的方向移动,即向正反应移动,H2的转化率提高,故C正确;
D、升温平衡向吸热的逆方向移动,故D正确.
故选CD.
点评:本题考查化学平衡图象、反应热计算、影响化学平衡与化学反应速率的因素等,难度中等,注意可逆反应表示的热化学方程式的意义.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
下列反应不属于氧化还原反应的是( )
A、3Fe+4H2O(g)
| ||||
| B、Cl2+2OH-═Cl-+ClO-+H2O | ||||
| C、Ca(OH)2+SO2═CaSO3+H2O | ||||
| D、2F2+2H2O═4HF+O2 |
下列对有机物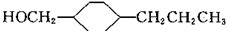 的说法,正确的是( )
的说法,正确的是( )
 的说法,正确的是( )
的说法,正确的是( )| A、属于芳香族化合物 |
| B、属于酚类物质 |
C、不能由有机物 催化加氢得到 催化加氢得到 |
D、能由有机物 催化加氢得到 催化加氢得到 |
下列说法正确的是( )
①氯水和液氯都能使干燥的有色布条褪色; ②食盐属于盐类,纯碱属于碱类;③冰和干冰既是纯净物又是化合物;④青铜和目前流通的1元硬币都是合金;⑤石油、甘油、豆油都属于油脂.
①氯水和液氯都能使干燥的有色布条褪色; ②食盐属于盐类,纯碱属于碱类;③冰和干冰既是纯净物又是化合物;④青铜和目前流通的1元硬币都是合金;⑤石油、甘油、豆油都属于油脂.
| A、①④ | B、③④ | C、③⑤ | D、②⑤ |
对1-18号元素中(除稀有气体元素外),下列说法错误的是( )
| A、原子半径最小的元素是氢 |
| B、非金属性最强的元素是氟 |
| C、碱性最强的最高价氧化物对应水化物是氢氧化钠 |
| D、气态氢化物中最稳定的是氯化氢 |
短周期主族元素A、B、C、D原子序数依次递增,A、B、D三种元素既不同周期也不同主族,且三元素原子的最外层电子数之和为13,B与C同周期,C的最外层电子数比B的最外层电子数多1.下列有关说法正确的是( )
| A、元素D的单质只能做氧化剂 |
| B、元素B和D可以形成化学式为BD3的共价化合物 |
| C、A、B两种元素形成的化合物的空间构型一定是三角锥形 |
| D、元素A、C不可能形成结构式为A-C-C-A的化合物 |
 如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )| A、1molH2中的化学键断裂时需要吸收436kJ能量 |
| B、2molHCl分子中的化学键形成时要释放862kJ能量 |
| C、稳定性:H2(g)>HCl(g) |
| D、此反应的热化学方程式为:H2(g)+Cl2(g)=2HCl(g)△H=-248kJ/mol |
碳纳米管和石墨烯(由石墨剥离的层状结构)经低温处理,获得了一种“最轻材料”.该材料具有超强的吸附能力,还有望成为理想的储能保温材料.下列有关说法正确的是( )
| A、石墨烯属于共价化合物 |
| B、该材料吸油过程为物理变化 |
| C、碳纳米管和石墨烯互为同位素 |
| D、碳纳米属于胶体分散系 |