题目内容
抗击“非典”期间过氧乙酸(
请回答下列问题:
(1)配平反应①的离子方程式(配平系数填入相应的方框内).
(2)用Na2S2O3标准液滴定I2时(反应④)选用的指示剂是________.
(3)取b0mL待测液,用H2SO4酸化,再用a1mol·L-1的标准KMnO4溶液滴定其中的H2O2,耗用KMnO4体积b1mL,(滴定过程中KMnO4不与![]() 反应)另取b0mL待测液,加入过量KI,用H2SO4酸化,
反应)另取b0mL待测液,加入过量KI,用H2SO4酸化,
此时![]()
与H2O2都能与KI反应生成I2(反应②和③).再用a2mol·L-1Na2S2O3标准液滴定生成I2,耗用Na2S2O3为b2mL.
请根据上述实验数据计算过氧乙酸浓度(用含a1,a2,b0,b1,b2的代数式表示).c0=___________
(4)为计算待测液中![]() 浓度c0,加入KI质量已过量但没有准确称量,是否影响测定结果________(填是或否).
浓度c0,加入KI质量已过量但没有准确称量,是否影响测定结果________(填是或否).
答案:
解析:
解析:
| 解析:本题考查的是有关氧化还原反应的一道试题
(1)根据电子得失守恒和电荷守恒关系可迅速解答 (2)检验淀粉溶液用碘水 (3)由以上离子方程式可知:n(CH3COOH)+n( 2.5a1b1,从而解得n(CH3COOH). (4)加入过量的KI溶液的目的是使过氧乙酸和双氧水全部反应,在进行计算时与KI的量无关. 答案:(1)2,5,6,2,5,8 (2)淀粉溶液 (3)
|

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目

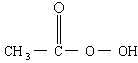 是广为使用的消毒剂.它可由
是广为使用的消毒剂.它可由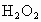 和冰醋酸反应制取,所以在过氧乙酸中常含有残留的
和冰醋酸反应制取,所以在过氧乙酸中常含有残留的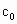 .涉及下列反应:
.涉及下列反应: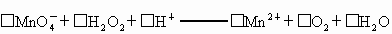
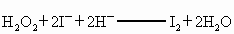
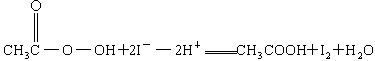


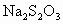 标准溶液滴定
标准溶液滴定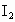 时(反应④)选用的指示剂是__________.
时(反应④)选用的指示剂是__________.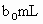 待测液,用硫酸使溶液酸化,再用浓度为
待测液,用硫酸使溶液酸化,再用浓度为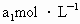 标准溶液滴定其中的
标准溶液滴定其中的 体积为
体积为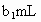 (反应①,滴定过程中
(反应①,滴定过程中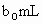 待测液,加入过量的KI,并用硫酸使溶液,酸化,此时过氧乙酸和残留的
待测液,加入过量的KI,并用硫酸使溶液,酸化,此时过氧乙酸和残留的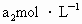 的
的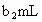 .
.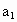 、
、 、
、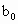 、
、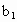 、
、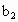 的代数式表示).
的代数式表示).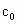 =__________.
=__________.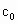 ,加入的KI的质量已过量,但没有准确称量,是否影响测定结果______(填“是”或“否”).
,加入的KI的质量已过量,但没有准确称量,是否影响测定结果______(填“是”或“否”).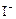 +2H+ =I2+2H2O
+2H+ =I2+2H2O 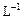 的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 L(反应①,滴定过程中KMnO4不与过氧乙酸反应)。另取b0 L待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2mol·
的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 L(反应①,滴定过程中KMnO4不与过氧乙酸反应)。另取b0 L待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2mol·