题目内容
将含NaCl杂质的5gNaOH样品配成1L溶液,测得此溶液的pH=13,请计算:
(1)该溶液中氢离子浓度是多少?
(2)该溶液中氢氧根离子浓度是多少?
(3)该溶液中氢氧化钠的物质的量浓度是多少?
(4)该溶液中氢氧化钠的物质的量是多少?
(5)该溶液中氢氧化钠的质量是多少?
(6)此样品的纯度(即样品中氢氧化钠的质量分数)是多少?
(1)该溶液中氢离子浓度是多少?
(2)该溶液中氢氧根离子浓度是多少?
(3)该溶液中氢氧化钠的物质的量浓度是多少?
(4)该溶液中氢氧化钠的物质的量是多少?
(5)该溶液中氢氧化钠的质量是多少?
(6)此样品的纯度(即样品中氢氧化钠的质量分数)是多少?
考点:物质的量浓度的相关计算
专题:
分析:(1)根据水的离子积计算出pH=13的氢氧化钠溶液中氢离子浓度;
(2)根据c(H+)=10-13mol/L及水的离子积计算出溶液中氢氧根离子浓度;
(3)NaOH为强电解质,该溶液中的氢氧根离子浓度为氢氧化钠的浓度;
(4)根据n=cV计算出溶液中氢氧化钠的物质的量;
(5)根据m=nM计算出氢氧化钠的质量;
(6)根据氢氧化钠的质量计算出氯化钠的质量,再计算出此样品的纯度.
(2)根据c(H+)=10-13mol/L及水的离子积计算出溶液中氢氧根离子浓度;
(3)NaOH为强电解质,该溶液中的氢氧根离子浓度为氢氧化钠的浓度;
(4)根据n=cV计算出溶液中氢氧化钠的物质的量;
(5)根据m=nM计算出氢氧化钠的质量;
(6)根据氢氧化钠的质量计算出氯化钠的质量,再计算出此样品的纯度.
解答:
解:(1)该溶液的pH=13,则溶液中中氢离子浓度为:c(H+)=10-13mol/L,
答:该溶液中氢离子浓度为10-13mol/L;
(2)该溶液中氢氧根离子浓度为:c(OH-)=
mol/L=0.1mol/L,
答:该溶液中氢氧根离子浓度为0.1mol/L;
(3)氢氧化钠为强电解质,该溶液中氢氧化钠的物质的量浓度与氢氧根离子浓度相等,则c(NaOH)=c(OH-)=0.1mol/L,
答:该溶液中氢氧化钠的物质的量浓度是0.1mol/L;
(4)该溶液中氢氧化钠的物质的量为:n(NaOH)=0.1mol/L×1L=0.1mol,
答:该溶液中氢氧化钠的物质的量是0.1mol;
(5)该溶液中氢氧化钠的质量为:40g/mol×0.1mol=4g,
答:该溶液中氢氧化钠的质量为4g;
(6)该样品中氢氧化钠的质量分数为:
×100%=80%,
答:此样品的纯度(即样品中氢氧化钠的质量分数)为80%.
答:该溶液中氢离子浓度为10-13mol/L;
(2)该溶液中氢氧根离子浓度为:c(OH-)=
| 1×10-14 |
| 1×10-13 |
答:该溶液中氢氧根离子浓度为0.1mol/L;
(3)氢氧化钠为强电解质,该溶液中氢氧化钠的物质的量浓度与氢氧根离子浓度相等,则c(NaOH)=c(OH-)=0.1mol/L,
答:该溶液中氢氧化钠的物质的量浓度是0.1mol/L;
(4)该溶液中氢氧化钠的物质的量为:n(NaOH)=0.1mol/L×1L=0.1mol,
答:该溶液中氢氧化钠的物质的量是0.1mol;
(5)该溶液中氢氧化钠的质量为:40g/mol×0.1mol=4g,
答:该溶液中氢氧化钠的质量为4g;
(6)该样品中氢氧化钠的质量分数为:
| 4g |
| 5g |
答:此样品的纯度(即样品中氢氧化钠的质量分数)为80%.
点评:本题考查了物质的量的有关计算、溶液pH的计算,题目难度不大,试题知识点较多,充分考查了学生的分析、理解能力及灵活应用所学知识的能力,明确物质的量与物质的量浓度、溶液酸碱性与溶液pH的关系为解答关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列气体属于温室效应气体的是( )
| A、CO2 |
| B、N2O |
| C、CH4 |
| D、N2 |
一定量的KClO3中加入浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,其中发生氧化反应的元素和发生还原反应的元素的质量之比为( )
| A、1:6 | B、6:1 |
| C、1:5 | D、5:1 |
有关食品添加剂的下列说法中正确的是( )
| A、食盐加碘,碘元素百分含量越高,食盐的质量越高 |
| B、菜炒熟出锅前再放碘盐以防分解,加醋会降低碘的利用率 |
| C、苯甲酸钠是常用的食品调味剂 |
| D、腌制肉食制品使用的亚硝酸盐即使不超标,也不可长期或大量的进食 |

 是一种合成药物的中间体,请写出以CH2(COOH)2、CH2Cl2 及
是一种合成药物的中间体,请写出以CH2(COOH)2、CH2Cl2 及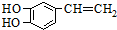 为原料制备该化合物,合成该化合物路线流程图(无机试剂任用),
为原料制备该化合物,合成该化合物路线流程图(无机试剂任用),