题目内容
在稀氨水中分别加入下列各种物质:A 氨水、B纯水、C少量浓硫酸、D少量氢氧化钠固体、E少量硫酸铝固体 (用字母填空)
(1)能使c(OH-)减少,使c(NH4+)增大的是 .
(2)能使c(OH-)增大,使c(NH4+)减小的是 .
(3)能使c(OH-)和c(NH4+)都增大的是 .
(4)能使c(OH-)和c(NH4+)都减小的是 .
(1)能使c(OH-)减少,使c(NH4+)增大的是
(2)能使c(OH-)增大,使c(NH4+)减小的是
(3)能使c(OH-)和c(NH4+)都增大的是
(4)能使c(OH-)和c(NH4+)都减小的是
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氨水中存在平衡NH3?H2O?NH4++OH-,
(1)使氢氧根离子浓度减小、铵根离子浓度增大,则加入的物质必须能和氢氧根离子反应;
(2)使氢氧根离子浓度增大、铵根离子浓度减小,则加入的物质必须含有氢氧根离子,能抑制氨水电离;
(3)使氢氧根离子和铵根离子浓度都增大,则加入的物质中必须含有铵根离子和氢氧根离子;
(4)使氢氧根离子和铵根离子浓度都减小,稀释溶液即可.
(1)使氢氧根离子浓度减小、铵根离子浓度增大,则加入的物质必须能和氢氧根离子反应;
(2)使氢氧根离子浓度增大、铵根离子浓度减小,则加入的物质必须含有氢氧根离子,能抑制氨水电离;
(3)使氢氧根离子和铵根离子浓度都增大,则加入的物质中必须含有铵根离子和氢氧根离子;
(4)使氢氧根离子和铵根离子浓度都减小,稀释溶液即可.
解答:
解:氨水中存在NH3?H2O?NH4++OH-,
①加入少量硫酸或硫酸铝,可生成水或氢氧化铝沉淀,使平衡向正向移动,则c(OH-)减少、c(NH4+)增大,故答案为:CE;
②能使c(OH-)增大、c(NH4+)减少,应加入碱或水解呈碱性的物质,则NaOH溶液以及少量K2CO3符合,故答案为:D;
③加入浓氨水,可使c(OH-)和c(NH4+)都增大,故答案为:A;
④加水稀释时,可使c(OH-)和c(NH4+)都减少,故答案为:B.
①加入少量硫酸或硫酸铝,可生成水或氢氧化铝沉淀,使平衡向正向移动,则c(OH-)减少、c(NH4+)增大,故答案为:CE;
②能使c(OH-)增大、c(NH4+)减少,应加入碱或水解呈碱性的物质,则NaOH溶液以及少量K2CO3符合,故答案为:D;
③加入浓氨水,可使c(OH-)和c(NH4+)都增大,故答案为:A;
④加水稀释时,可使c(OH-)和c(NH4+)都减少,故答案为:B.
点评:本题考查弱电解质的电离,为高频考点,侧重于学生的分析能力的考查,注意把握影响弱电解质的因素以及弱电解质的电离特点,注意相关基础知识的积累,难度不大.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
溶液和胶体的本质区别在于( )
| A、分散质微粒直径大小不同 |
| B、是否均一、稳定 |
| C、是否能发生丁达尔效应 |
| D、是否透明 |
可逆反应2A(g)+3B(g)?2C(g);△H=-QkJ?mol-1(Q>0).现有甲、乙两个容积相同且不变的真空密闭容器,向甲容器中加入2molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2 kJ;已知2Q1=Q2.下列叙述正确的( )
| A、平衡时甲、乙中C的体积分数甲>乙 |
| B、平衡时甲中A的转化率为60% |
| C、达到平衡后,再向乙中加入0.8molA+1.2molB+1.2molC,平衡向生成A的正向移动 |
| D、D甲容器达到平衡后,升温,反应的平衡常数增大 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2下列有关该电池的说法不正确的是( )
| A、电池的电解质溶液为碱性溶液,正极为Ni2O3、负极为Fe |
| B、电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C、电池放电过程中,溶液中的OH-向负极移动 |
| D、电池放电与充电过程发生的化学反应是可逆反应 |
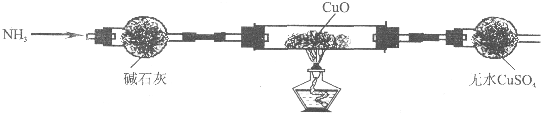
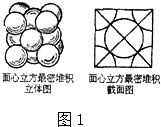 (1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是
(1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是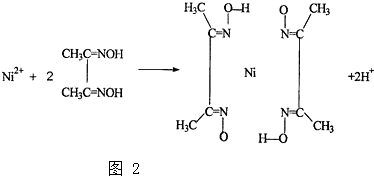
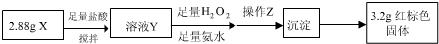
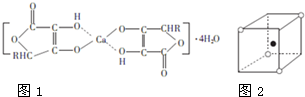 钙的化合物在共农业生产和生活中有广泛的应用.
钙的化合物在共农业生产和生活中有广泛的应用.