题目内容
有机化合物A含有C、H、O三种元素,取该有机物0.2mol 和0.9mol O2在密闭容器中燃烧,产物为CO、CO2和H2O(g),把产物依次通过浓硫酸、灼热的氧化铜和碱石灰.结果,浓H2SO4的质量重了18g,CuO的质量轻了9.6g,碱石灰的质量增重了35.2g.
(1)通过计算确定有机物A的分子式;
(2)若A可与金属钠反应生成氢气,且A分子中含有手性碳原子,请写出A的结构简式.
(1)通过计算确定有机物A的分子式;
(2)若A可与金属钠反应生成氢气,且A分子中含有手性碳原子,请写出A的结构简式.
分析:(1)浓硫酸具有吸水性,浓硫酸的质量增加18g说明反应产物中含水18g,通过灼热氧化铜,氧化铜质量减轻9.6g,结合方程式可计算CO的物质的量,通过碱石灰时,碱石灰的质量增加了35.2g可计算总CO2的物质的量,根据氧元素守恒可计算有机物中含有O的物质的量,进而求得化学式,并判断可能的结构简式;
(2)先根据手性碳原子指连有四个不同基团的碳原子,A可与金属钠反应生成氢气,说明有羟基,再根据分子式分析.
(2)先根据手性碳原子指连有四个不同基团的碳原子,A可与金属钠反应生成氢气,说明有羟基,再根据分子式分析.
解答:解:(1)浓硫酸增重18g说明反应产物中含水18g,即产物中含水
=1mol,
通过灼热氧化铜,氧化铜质量减轻9.6g,
CO+CuO
CO2+Cu△m
1mol 1mol 16g
0.6mol 0.6mol
=0.6mol
说明CO还原氧化铜反应中氧化铜失去O为9.6g,即0.6mol,
同时说明产物中含0.6molCO,
通过碱石灰增重35.2g说明还原氧化铜的得到的CO2与原产物的CO2总重35.2g,即0.8mol,减去由CO转化来的0.6moCO2,说明产物中含0.2molCO2.
通过上述分析,可以知道0.2mol有机物与 0.9mol氧气 反应生成1molH2O、0.6molCO、0.2molCO2,
即 2molH,2molO,0.8molC,减去参与反应的0.9molO2,即1.8molO,
可得知0.2mol 的有机物含有2molH,0.2molO,0.8molC,
即1mol有机物含10molH,1molO,4molC,化学式为C4H10O,
答:有机物的分子式为C4H10O;
(2)A可与金属钠反应生成氢气,说明有羟基,且A分子中含有手性碳原子,则有一个碳原子连有四个不同基团,所以其结构简式为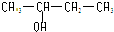 ;
;
答:有机物的结构简式为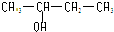 .
.
| 18g |
| 18g/mol |
通过灼热氧化铜,氧化铜质量减轻9.6g,
CO+CuO
| ||
1mol 1mol 16g
0.6mol 0.6mol
| 9.6g |
| 16g/mol |
说明CO还原氧化铜反应中氧化铜失去O为9.6g,即0.6mol,
同时说明产物中含0.6molCO,
通过碱石灰增重35.2g说明还原氧化铜的得到的CO2与原产物的CO2总重35.2g,即0.8mol,减去由CO转化来的0.6moCO2,说明产物中含0.2molCO2.
通过上述分析,可以知道0.2mol有机物与 0.9mol氧气 反应生成1molH2O、0.6molCO、0.2molCO2,
即 2molH,2molO,0.8molC,减去参与反应的0.9molO2,即1.8molO,
可得知0.2mol 的有机物含有2molH,0.2molO,0.8molC,
即1mol有机物含10molH,1molO,4molC,化学式为C4H10O,
答:有机物的分子式为C4H10O;
(2)A可与金属钠反应生成氢气,说明有羟基,且A分子中含有手性碳原子,则有一个碳原子连有四个不同基团,所以其结构简式为
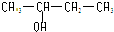 ;
;答:有机物的结构简式为
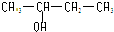 .
.点评:本题考查有机物分子式和结构简式的确定,题目难度不大,注意所含元素原子个数的计算角度,注意质量守恒定律的应用.

练习册系列答案
相关题目
 反应.
反应.



 +
+ +2H2O
+2H2O
 O4的质量重了18g ,CuO的质量轻了9.6g ,碱石灰的
O4的质量重了18g ,CuO的质量轻了9.6g ,碱石灰的