题目内容
 (1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H<0
C.2H2(g)+O2(g)═2H2O(l)△H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应为
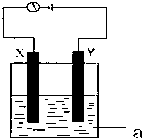
(3)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与如图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:
①若X和Y均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为
③若X、Y都是惰性电极,a是饱和NaCl溶液,则Y极的电极反应式为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)能设计成原电池的反应必须是自发进行的放热的氧化还原反应;
(2)碱性氢氧燃料电池中,负极上燃料氢气失电子好氢氧根离子反应生成水;
(3)①若X和Y均为惰性电极,a为CuSO4溶液,电解时,X电极上铜离子放电、Y电极上氢氧根离子放电;要使溶液恢复原状,应该根据“析出什么加入什么”原则加入物质,根据Cu和转移电子之间的关系式计算;
②若X、Y分别为铁和铜,a仍为CuSO4溶液,Y电极上铜失电子发生氧化反应;
③若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电;用湿润的淀粉碘化钾试纸检验氯气.
(2)碱性氢氧燃料电池中,负极上燃料氢气失电子好氢氧根离子反应生成水;
(3)①若X和Y均为惰性电极,a为CuSO4溶液,电解时,X电极上铜离子放电、Y电极上氢氧根离子放电;要使溶液恢复原状,应该根据“析出什么加入什么”原则加入物质,根据Cu和转移电子之间的关系式计算;
②若X、Y分别为铁和铜,a仍为CuSO4溶液,Y电极上铜失电子发生氧化反应;
③若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电;用湿润的淀粉碘化钾试纸检验氯气.
解答:
解:(1)A.该反应在吸热反应,不能设计成原电池,故错误;
B.该反应不属于氧化还原反应,不能设计成原电池,故错误;
C.该反应属于自发进行的放热的氧化还原反应,能设计成原电池,故正确;
故选C;
(2)碱性氢氧燃料电池中,负极上燃料氢气失电子好氢氧根离子反应生成水,电极反应式为H2-2e-+2OH-=2H2O,故答案为:H2-2e-+2OH-=2H2O;
(3)①若X和Y均为惰性电极,a为CuSO4溶液,电解时,X电极上铜离子放电、Y电极上氢氧根离子放电,所以电池反应式为2CuSO4+2H2O
2Cu+O2↑+2H2SO4;加入0.2molCuO能使溶液恢复原状,说明电解过程中只生成氧气和铜,根据Cu原子守恒得n(CuO)=n(Cu)=0.2mol,根据Cu和转移电子之间的关系知,转移电子的物质的量=0.2mol×2=0.4mol,
故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;0.4mol;
②若X、Y分别为铁和铜,a仍为CuSO4溶液,Y电极上铜失电子发生氧化反应,电极反应式为Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
③若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电,电极反应式为2Cl --2e -=Cl2↑;用湿润的淀粉碘化钾试纸检验氯气,其检验方法为把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色则有Cl2生成,
故答案为:2Cl --2e -=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色则有Cl2生成.
B.该反应不属于氧化还原反应,不能设计成原电池,故错误;
C.该反应属于自发进行的放热的氧化还原反应,能设计成原电池,故正确;
故选C;
(2)碱性氢氧燃料电池中,负极上燃料氢气失电子好氢氧根离子反应生成水,电极反应式为H2-2e-+2OH-=2H2O,故答案为:H2-2e-+2OH-=2H2O;
(3)①若X和Y均为惰性电极,a为CuSO4溶液,电解时,X电极上铜离子放电、Y电极上氢氧根离子放电,所以电池反应式为2CuSO4+2H2O
| ||
故答案为:2CuSO4+2H2O
| ||
②若X、Y分别为铁和铜,a仍为CuSO4溶液,Y电极上铜失电子发生氧化反应,电极反应式为Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
③若X、Y都是惰性电极,a是饱和NaCl溶液,Y电极上氯离子放电,电极反应式为2Cl --2e -=Cl2↑;用湿润的淀粉碘化钾试纸检验氯气,其检验方法为把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色则有Cl2生成,
故答案为:2Cl --2e -=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色则有Cl2生成.
点评:本题考查了原电池和电解池原理,根据原电池反应特点及各个电极上发生的反应来分析解答,氯气的检验方法、电极反应式书写等都是考查热点,注意(3)②活泼金属作阳极时发生的电极反应,为易错点.

练习册系列答案
相关题目
元素X和元素Y在周期表中位于相邻的两个周期:X与Y两原子核外电子总数之和为19;Y的原子核内质子数比X多3个.下列描述中不正确的是( )
| A、X与Y形成的化合物的化学式可能为Y2X2 |
| B、X的化合物种类比Y的化合物种类多 |
| C、Y能置换出酸中的氢,却不能置换出盐溶液中的金属 |
| D、X和Y都是性质很活泼的元素,在自然界中都只能以化合态形式存在 |
某二元酸(H2A)在水中的电离方程式为:H2A═H++HA- HA-?H++A2-(Ka=1.0×10-2),下列说法正确的是( )
| A、在0.1mol?L-1的H2A溶液中,c(H+)>0.12mol?L-1 |
| B、在0.1mol?L-1的Na2A溶液中,c(A2-)+c(HA-)+c(Na+)=0.2mol?L-1 |
| C、分别将同浓度(0.1mol?L-1)的NaHA和Na2A溶液等体积混合,其pH一定小于7 |
| D、0.1mol?L-1的NaHA溶液中离子浓度为:c(Na+)>c(H+)>c(HA-)>c(A2-)>c(OH-) |
下列离子方程式书写正确的是( )
| A、向NH4HCO3溶液中加过量Ca(OH)2溶液:HCO3-+OH-+Ca2+═CaCO3↓+H2O | ||||
B、用惰性电极MgCl2电解水溶液:2Cl-+2H2O
| ||||
| C、向偏铝酸钠溶液中加入少量硫酸氢钠溶液:AlO2-+H++H2O═Al(OH)3↓ | ||||
| D、浓盐酸跟二氧化锰混合共热:MnO2+4H++4Cl-═MnO2++2H2O+2Cl2 |
