题目内容
13.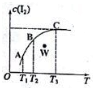 将I2溶于KI溶液中,能配制成浓度较大的碘水,主要是发生了反应:I2(aq)+I-(aq)?I3-(aq),该平衡体系中,I2的物质的量浓度与温度(T)的关系如图所示(曲线上的任何一点都代表平衡状态),下列说法正确的是( )
将I2溶于KI溶液中,能配制成浓度较大的碘水,主要是发生了反应:I2(aq)+I-(aq)?I3-(aq),该平衡体系中,I2的物质的量浓度与温度(T)的关系如图所示(曲线上的任何一点都代表平衡状态),下列说法正确的是( )| A. | 正反应为吸热反应 | B. | 平衡常数:KA>KB | ||
| C. | 反应速率:vB>vC | D. | W点时,v正>v逆 |
分析 A.根据温度升高时平衡移动的方向判断该反应的反应热;
B.该反应为放热反应,温度升高,平衡向着逆向移动,则化学平衡常数减小;
C.温度对反应速率影响较大,温度越高,反应速率越快;
D.W点没有达到平衡状态,此时碘单质的浓度小于平衡状态,则反应向着逆向移动,据此判断反应速率大小.
解答 解:A.随着温度的不断升高,I2的物质的量浓度,说明反应向逆方向移动,则I2(aq)+I-(aq)?I3-(aq)为放热反应,故A错误;
B.I2(aq)+I-(aq)?I3-(aq)为放热反应,温度升高,平衡向着逆向移动,则反应物浓度减小、生成物浓度增大,化学平衡常数减小,由于温度A<B,则平衡常数:KA>KB,故B正确;
C.温度越大,反应速率越快,由于C点温度大于B,则反应速率:vB>vC,故C错误;
D.W点没有达到平衡状态,I2的浓度小于平衡状态,则反应向着逆向移动,v正<v逆,故D错误;
故选B.
点评 本题考查化学平衡的移动和平衡常数的运用,题目难度中等,注意化学平衡图象分析的一般方法来解答:一看面:看清图象中横坐标和纵坐标的含义;二看线:弄清图象中线的斜率或线走势的意义;三看点:明确曲线的起点、终点、交点及拐点等;四看是否需要辅助线,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
12.丙烯酸的结构简式为CH2=CH-COOH,下列关于丙烯酸的说法错误的是( )
| A. | 丙烯酸可以发生取代反应 | |
| B. | 丙烯酸可以使酸性高锰酸钾溶液褪色 | |
| C. | 丙烯酸与HBr发生加成反应只能得到唯一产物 | |
| D. | 丙烯酸钠溶液中Na+浓度大于丙烯酸根离子浓度 |
4.一定质量的混合气体在密闭容器中发生如下反应:xA(气)+yB(气)?zC(气).达到平衡后,测得A气体的浓度为0.5mol/L.当恒温下将密闭容器的容积扩大到原来的二倍,再达平衡后,测得A的浓度为0.3mol/L.下列叙述正确的是( )
| A. | 平衡向正反应方向移动 | B. | x+y>z | ||
| C. | C的体积分数增大 | D. | B的转化率增大 |
5.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 500 mL1 mol/L MgCl2溶液中含有Cl-数目为0.5NA | |
| B. | 标准状况下,33.6L SO3与48gO2所占的体积相等 | |
| C. | 17 gNH3含有的电子个数为l0NA | |
| D. | 1 mol O2与2 mol SO2一定条件下混合反应,可生成2 mol SO3 |
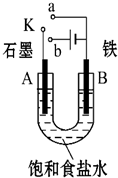 某课外活动小组用如图装置进行实验,试回答下列问题.
某课外活动小组用如图装置进行实验,试回答下列问题.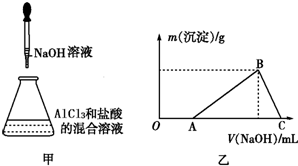 某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.
某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.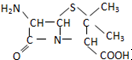 ) 是青霉素类抗生素的母核,与有机物F缩合生成阿莫西林.某同学用对甲基苯酚为原料设计阿莫西林的合成路线如图:
) 是青霉素类抗生素的母核,与有机物F缩合生成阿莫西林.某同学用对甲基苯酚为原料设计阿莫西林的合成路线如图: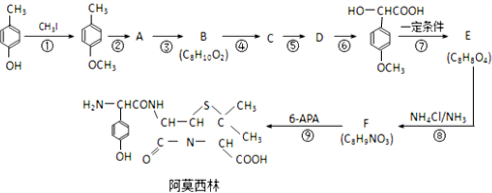
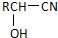 $\stackrel{H_{2}O/H+}{→}$
$\stackrel{H_{2}O/H+}{→}$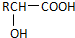
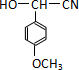 ;
;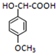 的一种同分异构体的一氯代物的结构为
的一种同分异构体的一氯代物的结构为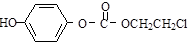 ,该物质在NaOH水溶液中加热反应反应时的化学方程式为
,该物质在NaOH水溶液中加热反应反应时的化学方程式为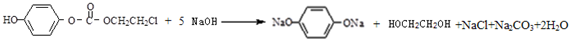 ;
;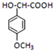 满足以下条件的同分异构体有3种.
满足以下条件的同分异构体有3种.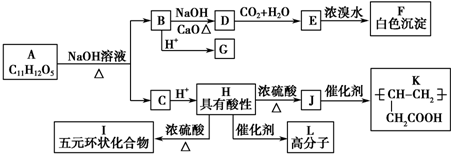
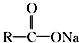 +NaOH$→_{△}^{CaO}$R═H+Na2CO3
+NaOH$→_{△}^{CaO}$R═H+Na2CO3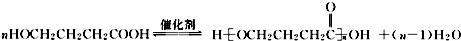 .
. .
.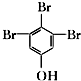 (写结构简式).
(写结构简式).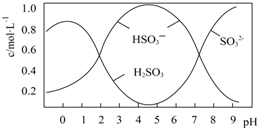 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂.