题目内容
下列叙述不正确的是( )
| A.足量的硫单质与64g铜反应,有1mol电子发生转移 |
| B.虽然SiO2是酸性氧化物,但SiO2与某酸反应 |
| C.Mg比Al活泼,在Mg和Al形成的原电池中,Mg不一定作负极 |
| D.Na2O2与CO2反应生成Na2CO3和O2,SO2和Na2O2反应生成Na2SO3和O2 |
A、硫单质与铜反应生成硫化亚铜,铜的化合价由0价升高为+1价,64g铜为1mol,转移电子物质的量等于铜的物质的量为1mol,故A正确;
B、酸性氧化物一般不酸反应,SiO2是酸性氧化物,但能与氢氟酸反应,故B正确;
C、原电池中负极发生氧化反应,正极发生还原反应,Mg和Al为电极,NaOH溶液为电解质溶液,形成的原电池,实质是铝与氢氧化钠反应生成偏铝酸钠与氢气,Al作负极,以盐酸为电解质溶液,Mg作负极,故C正确;
D、SO2有较强的还原性,Na2O2有强氧化性,SO2和Na2O2发氧化还原反应,过氧化钠被还原,不产生氧气,故D错误.
故选D.
B、酸性氧化物一般不酸反应,SiO2是酸性氧化物,但能与氢氟酸反应,故B正确;
C、原电池中负极发生氧化反应,正极发生还原反应,Mg和Al为电极,NaOH溶液为电解质溶液,形成的原电池,实质是铝与氢氧化钠反应生成偏铝酸钠与氢气,Al作负极,以盐酸为电解质溶液,Mg作负极,故C正确;
D、SO2有较强的还原性,Na2O2有强氧化性,SO2和Na2O2发氧化还原反应,过氧化钠被还原,不产生氧气,故D错误.
故选D.

练习册系列答案
相关题目
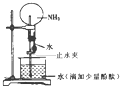 如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )| A、该实验说明氨气是一种极易溶于水的气体 | B、进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性 | C、氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化 | D、形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压 |
苯与乙烯相比较,下列叙述不正确的是( )
| A、都能燃烧,生成二氧化碳和水 | B、都容易发生加成反应 | C、乙烯易发生加成反应,苯只能在特殊条件下才发生加成反应 | D、乙烯易被酸性高锰酸钾溶液氧化,苯不能被酸性高锰酸钾溶液氧化 |