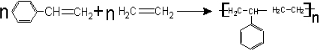题目内容
17.下列说法正确的是( )| A. | 将22.4 L HCl溶于水配制1 L溶液,其溶质的物质的量浓度为1.0 mol/L | |
| B. | 1 mol/L的Na2CO3溶液中含有2 mol Na+ | |
| C. | 500 mL 0.5 mol/L的(NH4)2SO4溶液中含有NH4+个数为0.5NA(NA为阿伏加德罗常数) | |
| D. | Na+浓度为0.2 mol/L的Na2SO4溶液中SO42-浓度为0.1 mol/L |
分析 A.未说明标况,无法求出HCl的物质的量;
B.缺少溶液的体积,无法计算;
C.铵根离子属于弱碱的阳离子,会发生水解;
D.由化学式可知,Na+浓度与SO42-浓度之比为2:1.
解答 解:A.未说明标况,无法求出HCl的物质的量,所以也就无法求出溶质的物质的量浓度,故A错误;
B.1mol/L的Na2CO3溶液中钠离子的物质的量浓度为2mol/L,缺少溶液的体积,无法计算出钠离子的物质的量,故B错误;
C.弱碱的阳离子铵根离子要发生水解,500mL 0.5mol/L的(NH4)2SO4溶液中含有NH4个数为小于0.5NA(NA为阿伏加德罗常数),故C错误;
D.由化学式可知,Na+浓度与SO42-浓度之比为2:1,所以Na+浓度为0.2mol/L的Na2SO4溶液中SO42-浓度为0.1mol/L,故D正确;
故选D.
点评 本题考查物质的量浓度有关计算,题目难度较小,注意公式的使用条件,C需考虑盐类的水解,为易错点.

练习册系列答案
相关题目
19.某原电池结构如图所示,下列有关该装置的说法正确的是( )
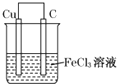

| A. | 将电能转换成化学能 | |
| B. | 碳棒上发生氧化反应 | |
| C. | 溶液中Cl-向铜棒一极移动 | |
| D. | 发生的总反应为:3Cu+2Fe3+═2Fe+3Cu2+ |
5.下列表示物质结构的化学用语或模型正确的是( )
| A. | 甲酸甲酯的结构简式:C2H4O2 | B. | H2O2的电子式: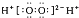 | ||
| C. | 中子数为10 的氧原子:188O | D. | 对-硝基甲苯的结构简式: |
12.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族.下列说法正确的是( )
| A. | 元素Y、W的简单阴离子具有相同的电子层结构 | |
| B. | 由X、W两种元素组成的化合物是离子化合物 | |
| C. | X的简单气态氢化物的热稳定性比W的强是因为X的氢化物分子间易形成氢键 | |
| D. | 离子半径:r(Z)<r(Y)<r(X)<r(W) |
2.如表中对于相关物质的分类全部正确的一组是( )
| 编号 | 纯净物 | 混合物 | 弱电解质 | 非电解质 |
| A | 明矾 | 铝热剂 | BaSO4 | CO2 |
| B | 氨水 | 石膏 | SO2 | CH3CH2OH |
| C | 苏打 | 氢氧化铁胶体 | H2SiO3 | NH3 |
| D | 胆矾 | 钢铁 | H2CO3 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
9.下列过程属于物理变化的是( )
| A. | 石油的分馏 | B. | 石油的裂化 | C. | 煤的干馏 | D. | 乙烯聚合 |
6.海边的铁制品比较容易生锈,月球上的铁不易腐蚀.钢铁发生腐蚀时,正极上发生的反应为( )
| A. | 2Fe-4e-═2Fe2+ | B. | 2Fe2++4e-═2Fe | ||
| C. | 2H2O+O2+4e-═4OH- | D. | 2Fe3++2e-═2Fe2+ |
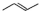 .
.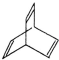 ,该有机物与H2加成时最多能消耗氢气的物质的量3mol,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式
,该有机物与H2加成时最多能消耗氢气的物质的量3mol,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式 ,将Y加入酸性高锰酸钾溶液中的现象酸性高锰酸钾溶液褪色.
,将Y加入酸性高锰酸钾溶液中的现象酸性高锰酸钾溶液褪色.