题目内容
25℃时将10mLpH=11的氨水加水稀释至100mL,下列判断正确的是( )
| A、稀释后溶液的pH=7 | ||||
| B、氨水的电离度增大,溶液中所有离子的浓度均减小 | ||||
C、稀释过程中
| ||||
| D、pH=11氨水的浓度为0.001mol/L |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A.一水合氨是弱电解质,在水溶液里部分电离,加水促进电离;
B.加水稀释促进一水合氨电离,溶液中c(H+)增大;
C.加水稀释氨水,促进一水合氨电离,导致溶液中n(NH4+)增大、n(NH3.H2O)减小;
D.溶液中氨水浓度大于氢氧根离子的浓度.
B.加水稀释促进一水合氨电离,溶液中c(H+)增大;
C.加水稀释氨水,促进一水合氨电离,导致溶液中n(NH4+)增大、n(NH3.H2O)减小;
D.溶液中氨水浓度大于氢氧根离子的浓度.
解答:
解:A.一水合氨是弱电解质,在水溶液里部分电离,加水促进电离,将10mLpH=11的氨水加水稀释至100mL,体积增大10倍,pH变化小于1个单位,即稀释后10<pH<11,故A错误;
B.加水稀释促进一水合氨电离,溶液中c(OH-)减小,温度不变,则水的离子积常数不变,则溶液中c(H+)增大,故B错误;
C.加水稀释氨水,促进一水合氨电离,导致溶液中n(NH4+)增大、n(NH3.H2O)减小,则溶液中
增大,故C正确;
D.一水合氨是弱电解质,在水溶液里部分电离,则溶液中氨水浓度大于氢氧根离子的浓度,则pH=11氨水的浓度大于0.001mol/L,故D错误;
故选C.
B.加水稀释促进一水合氨电离,溶液中c(OH-)减小,温度不变,则水的离子积常数不变,则溶液中c(H+)增大,故B错误;
C.加水稀释氨水,促进一水合氨电离,导致溶液中n(NH4+)增大、n(NH3.H2O)减小,则溶液中
c(N
| ||
| c(NH3?H2O) |
D.一水合氨是弱电解质,在水溶液里部分电离,则溶液中氨水浓度大于氢氧根离子的浓度,则pH=11氨水的浓度大于0.001mol/L,故D错误;
故选C.
点评:本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,注意稀释氨水过程中增大一水合氨电离程度但其电离平衡常数不变,溶液中c(H+)增大,为易错点.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀.则下列说法不正确的是( )
| A、原合金中含0.1mol Fe、0.15mol Cu |
| B、25.4g沉淀为Cu(OH)2和Fe(OH)3的混合物 |
| C、气体X中含0.3 mol NO、0.1 mol NO2 |
| D、气体X中含0.3 mol NO2、0.1 mol NO |
下述实验方案能达到实验目的是.( )
| 编号 | A | B | C | D |
| 实验 方案 |  | 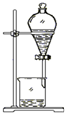 | 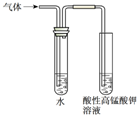 | 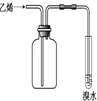 |
| 实验 目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
| A、A | B、B | C、C | D、D |
下列实验能达到预期目的是( )
| A、检验溶液中是否含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 |
| B、检验溶液中是否含有SO42-:先滴加氯化钡溶液,再滴加稀盐酸 |
| C、检验溶液中是否含有Fe2+:先滴加氯水,再滴加KSCN溶液 |
| D、检验溶液中是否含有NH4+:先滴加浓NaOH溶液并加热,再用湿润的红色石蕊试纸 |
下列水溶液中,能大量共存的一组离子是( )
| A、Na+、H+、NO3-、SO32- |
| B、K+、H+、SO42-、CH3COO- |
| C、Mg2+、NH4+、SO42-、Cl- |
| D、K+、Fe3+、Cl-、SCN- |

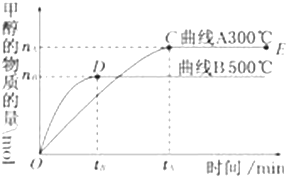 (1)一定条件下,在体积为4L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g).
(1)一定条件下,在体积为4L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g).