题目内容
17.常温下,物质的量浓度相等的下列物质的水溶液,PH最小的是( )| A. | NaOH | B. | FeCl3 | C. | Na2CO3 | D. | NaCl |
分析 相同物质的量浓度的下列物质的稀溶液中,pH最小,说明该溶液酸性最大,根据弱电解质的电离、盐类水解分析解答.
解答 解:A.NaOH是强碱,其水溶液显强碱性;
B.FeCl3是强酸弱碱盐,在溶液中水解显酸性;
C.Na2CO3是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性;
D.NaCl强酸强碱盐,在溶液中显中性,
通过以上分析知,这几种物质酸性最强的是FeCl3;
故选B.
点评 本题考查溶液酸碱性大小比较,为高频考点,明确弱电解质电离特点及盐类特点是解本题关键,知道常见酸的酸性强弱,题目难度不大.

练习册系列答案
相关题目
6.如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O,下列关于该电池工作时的说法正确的是( )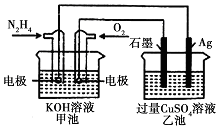

| A. | 该装置工作时,Ag电极上有气体生成 | |
| B. | 甲池和乙池中的溶液的pH均减小 | |
| C. | 甲池中负极反应为N2H4-4e-═N2+4H+ | |
| D. | 当甲池中消耗0.1molN2H4时,乙池中理沦上最多产生6.4g固体 |
2.实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
| A. | 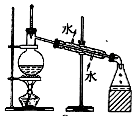 装置常用于分离互不相溶的液体混合物 | |
| B. | 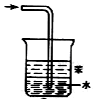 装置可用于吸收氨气,且能防止倒吸 | |
| C. | 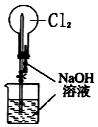 用装置不可以完成“喷泉”实验 | |
| D. | 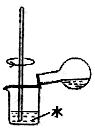 用装置稀释浓硫酸和铜反应冷却后的混合液 |
9.下列关于钠的说法中不正确的是( )
| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 钠长期放置在空气中,最终将变成碳酸钠 | |
| C. | 钠的化学性质比较活泼,少量的钠可以保存在与钠不反应的煤油中 | |
| D. | 将一小块钠投入氯化铁溶液时,既能产生气体又会出现白色沉淀 |
6.在日光的照射下,下列物质不发生化学变化的是( )
| A. | 浓HNO3 | B. | H2和N2的混合气 | C. | 溴化银 | D. | 氯水 |