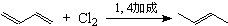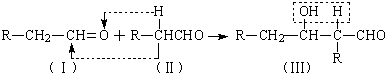题目内容
维拉佐酮是临床上使用广泛的抗抑郁药,其关键中间体合成路线如图: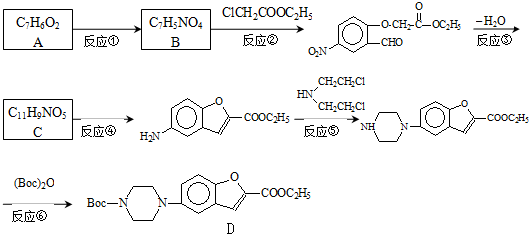
已知:① ;
;
②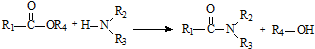 .
.
(1)反应类型:反应④ ;反应⑤ .
(2)结构简式:A ;C .
(3)书写反应②的化学方程式: .实验中反应②必须在K2CO3弱碱性条件下进行的原因是 .
(4)合成过程中反应③与反应④不能颠倒的理由为: .
(5)反应⑥中(Boc)2O是由两分子C5H10O3脱水形成的酸酐,写出分子式为C5H10O3,其同分异构体分子中只含有2种不同化学环境氢原子,能发生水解反应的结构简式(书写2种): 、 .
(6)实验室还可用 和
和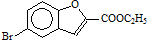 直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式 .
直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式 .

已知:①
 ;
;②
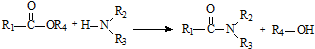 .
.(1)反应类型:反应④
(2)结构简式:A
(3)书写反应②的化学方程式:
(4)合成过程中反应③与反应④不能颠倒的理由为:
(5)反应⑥中(Boc)2O是由两分子C5H10O3脱水形成的酸酐,写出分子式为C5H10O3,其同分异构体分子中只含有2种不同化学环境氢原子,能发生水解反应的结构简式(书写2种):
(6)实验室还可用
 和
和 直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式
直接反应生成D,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)(2)根据A到B再到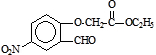 ,对比分子式与有机物的结构,可知A为
,对比分子式与有机物的结构,可知A为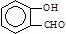 ,B为
,B为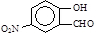 ,反应①为硝化反应,反应②为取代反应.而由
,反应①为硝化反应,反应②为取代反应.而由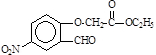 到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为
到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为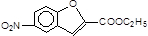 ,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代;
,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代;
(3)反应②B中酚羟基氢原子被-CH2COOC2H5取代,还有HCl生成;从化学平衡移动的角度进行考虑实验中反应②必须在K2CO3弱碱性条件下进行的原因;
(4)由于醛基可以被还原为羟基,故合成过程中反应③与反应④不能颠倒;
(5)能发生水解反应,说明是酯类,且分子中只含有2种不同化学环境氢原子,结合分子式可知,可以是碳酸与2-甲基-2-丙醇形成酯,也可以是碳酸与乙醇形成的酯;
(6)由信息可知,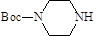 中氨基中的氢被
中氨基中的氢被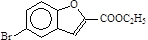 中的类似于信息2中基团取代,同时生成乙醇.
中的类似于信息2中基团取代,同时生成乙醇.
 ,对比分子式与有机物的结构,可知A为
,对比分子式与有机物的结构,可知A为 ,B为
,B为 ,反应①为硝化反应,反应②为取代反应.而由
,反应①为硝化反应,反应②为取代反应.而由 到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为
到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为 ,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代;
,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代;(3)反应②B中酚羟基氢原子被-CH2COOC2H5取代,还有HCl生成;从化学平衡移动的角度进行考虑实验中反应②必须在K2CO3弱碱性条件下进行的原因;
(4)由于醛基可以被还原为羟基,故合成过程中反应③与反应④不能颠倒;
(5)能发生水解反应,说明是酯类,且分子中只含有2种不同化学环境氢原子,结合分子式可知,可以是碳酸与2-甲基-2-丙醇形成酯,也可以是碳酸与乙醇形成的酯;
(6)由信息可知,
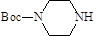 中氨基中的氢被
中氨基中的氢被 中的类似于信息2中基团取代,同时生成乙醇.
中的类似于信息2中基团取代,同时生成乙醇.解答:
解:根据A到B再到 ,对比分子式与有机物的结构,可知A为
,对比分子式与有机物的结构,可知A为 ,B为
,B为 ,反应①为硝化反应,反应②为取代反应.而由
,反应①为硝化反应,反应②为取代反应.而由 到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为
到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为 ,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代,
,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代,
(1)反应④发生的是硝基还原为氨基的反应,属于还原反应;对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,故答案为:还原反应;取代反应;
(2)由上述分析可知,A的结构简式为 ,C的结构简式为
,C的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
(3)反应②B中酚羟基氢原子被-CH2COOC2H5取代,还有HCl生成,反应方程式为: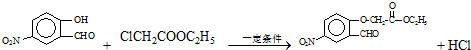 ;
;
实验中反应②必须在K2CO3弱碱性条件下进行,从化学平衡移动的角度进行考虑:弱碱性下K2CO3可与生成的HCl反应,使反应②更多的向正反应方向移动,
故答案为: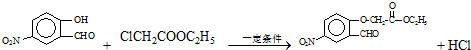 ;弱碱性下K2CO3可与生成的HCl反应,使反应②更多的向正反应方向移动;
;弱碱性下K2CO3可与生成的HCl反应,使反应②更多的向正反应方向移动;
(4)由于醛基可以被还原为羟基,故合成过程中反应③与反应④不能颠倒,目的是:防止醛基被还原,故答案为:防止醛基被还原;
(5)能发生水解反应,说明是酯类,且分子中只含有2种不同化学环境氢原子,结合分子式可知,可以是碳酸与2-甲基-2-丙醇形成酯,也可以是碳酸与乙醇形成的酯,相应的结构简式为: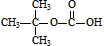 和
和 ,故答案为:
,故答案为: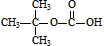 和
和 ;
;
(6)由信息可知,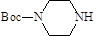 中氨基中的氢被
中氨基中的氢被 中的类似于信息2中基团取代,同时生成乙醇,故副产物的结构简式为
中的类似于信息2中基团取代,同时生成乙醇,故副产物的结构简式为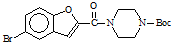 、C2H5OH,故答案为:
、C2H5OH,故答案为: 、C2H5OH.
、C2H5OH.
 ,对比分子式与有机物的结构,可知A为
,对比分子式与有机物的结构,可知A为 ,B为
,B为 ,反应①为硝化反应,反应②为取代反应.而由
,反应①为硝化反应,反应②为取代反应.而由 到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为
到C物质,脱掉一分子水,再对比C前、后物质的结构,可推出C为 ,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代,
,反应④发生的是硝基还原为氨基的反应,对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,对比反应⑥中反应物、产物结构可知,N原子上的H原子被取代,(1)反应④发生的是硝基还原为氨基的反应,属于还原反应;对比反应⑤中反应物、产物的结构可知,发生类似信息的反应,为取代反应,故答案为:还原反应;取代反应;
(2)由上述分析可知,A的结构简式为
 ,C的结构简式为
,C的结构简式为 ,故答案为:
,故答案为: ;
; ;
;(3)反应②B中酚羟基氢原子被-CH2COOC2H5取代,还有HCl生成,反应方程式为:
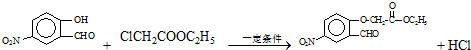 ;
;实验中反应②必须在K2CO3弱碱性条件下进行,从化学平衡移动的角度进行考虑:弱碱性下K2CO3可与生成的HCl反应,使反应②更多的向正反应方向移动,
故答案为:
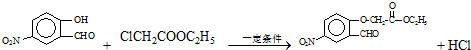 ;弱碱性下K2CO3可与生成的HCl反应,使反应②更多的向正反应方向移动;
;弱碱性下K2CO3可与生成的HCl反应,使反应②更多的向正反应方向移动;(4)由于醛基可以被还原为羟基,故合成过程中反应③与反应④不能颠倒,目的是:防止醛基被还原,故答案为:防止醛基被还原;
(5)能发生水解反应,说明是酯类,且分子中只含有2种不同化学环境氢原子,结合分子式可知,可以是碳酸与2-甲基-2-丙醇形成酯,也可以是碳酸与乙醇形成的酯,相应的结构简式为:
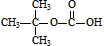 和
和 ,故答案为:
,故答案为: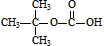 和
和 ;
;(6)由信息可知,
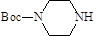 中氨基中的氢被
中氨基中的氢被 中的类似于信息2中基团取代,同时生成乙醇,故副产物的结构简式为
中的类似于信息2中基团取代,同时生成乙醇,故副产物的结构简式为 、C2H5OH,故答案为:
、C2H5OH,故答案为: 、C2H5OH.
、C2H5OH.
点评:本题考查有机物的合成,充分利用有机物的结构与分子式进行分析解答,较好的考查学生的分析推理、综合运用知识的能力,需要学生具备扎实的基础,难度中等.

练习册系列答案
相关题目
下列有关对晶体的判断正确的是( )
| A、熔点MgO>NaCl>KCl |
| B、含有金属阳离子的晶体一定是离子晶体 |
| C、同主族元素形成的氧化物的晶体类型均相同 |
| D、沸点:H2O>PH3>NH3 |
工业上由重晶石制取可溶性钡盐,对已经粉碎后的矿石首先进行的处理方法应是( )
| A、水溶法 | B、酸溶法 |
| C、碱溶法 | D、还原法 |