题目内容
10.有机物A可用作果实催熟剂.某同学欲以A为主要原料合成乙酸乙酯,其合成路线如图所示.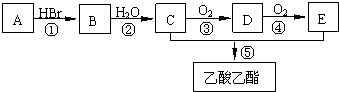
请回答:
(1)C的结构简式是CH3CH2OH,分子中含有的官能团名称是羟基;C的同分异构体F的核磁共振氢谱中,只有一种类型氢原子的吸收峰,F的结构简式是CH3OCH3.
(2)反应①的反应类型是加成反应,反应 ②~⑤中反应类型相同的是②和⑤、③和④(填序号).
(3)由A可以直接可以直接被转化为C,其反应的化学方程式是:CH2=CH2+H2O $→_{△}^{催化剂}$CH3CH2OH.
(4)反应②的化学方程式是2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH,反应④的化学方程式是2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH.
(5)取少量样品B,为了检验B中的溴元素,以下操作合理的顺序是bcda(填序号).
a.加AgNO3溶液 b.加NaOH 溶液 c.加热 d.加稀硝酸至溶液显酸性.
分析 C连续氧化得到E,二者反应得到CH3COOCH2CH3,则C为CH3CH2OH,E为CH3COOH,乙醇发生氧化反应生成D为CH3CHO,乙醛进一步发生氧化反应生成CH3COOH,有机物A可用作果实催熟剂,系列转化得到CH3CH2OH,故A为C2H4,与水发生加成反应得到B为CH3CH2Br,溴乙烷发生水解反应得到CH3CH2OH,据此解答.
解答 解:C连续氧化得到E,二者反应得到CH3COOCH2CH3,则C为CH3CH2OH,E为CH3COOH,乙醇发生氧化反应生成D为CH3CHO,乙醛进一步发生氧化反应生成CH3COOH,有机物A可用作果实催熟剂,系列转化得到CH3CH2OH,故A为C2H4,与水发生加成反应得到B为CH3CH2Br,溴乙烷发生水解反应得到CH3CH2OH,
(1)C为CH3CH2OH,C分子中含有的官能团名称是羟基,C的同分异构体的核磁共振氢谱只有一种类型氢原子的吸收峰,其结构简式是CH3OCH3,
故答案为:CH3CH2OH;羟基;CH3OCH3;
(2)反应①是乙烯与HBr发生加成反应,反应②⑤均属于取代反应,反应③④均是氧化反应,
故答案为:加成;②⑤;③④;
(3)由A直接转化为C的化学方程式是 CH2=CH2+H2O $→_{△}^{催化剂}$CH3CH2OH,
故答案为:CH2=CH2+H2O $→_{△}^{催化剂}$CH3CH2OH;
(4)反应②的化学方程式是CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr,反应④的化学方程式是 2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH,
故答案为:CH3CH2Br+NaOH$→_{△}^{水}$CH3CH2OH+NaBr;2CH3CHO+O2 $\stackrel{催化剂}{→}$2CH3COOH;
(5)检验B中的溴元素,可以将B在碱性条件下水解,再酸化后加AgNO3溶液,若出现淡黄色沉淀,则有溴元素,所以操作的顺序是bcda,
故答案为:bcda.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸的性质与转化,比较基础,侧重对基础知识的巩固.

| A. | 常温常压下,23gNO2含有NA个氧原子 | |
| B. | 常温常压下,18mLH2O约含有NA个H2O分子 | |
| C. | 含14 NA个电子的N2分子的物质的量是1mol | |
| D. | 0.1mol/L的Ba(OH)2溶液中,OH-的个数为0.2NA个 |
| A. | C2H6 C2H4 C2H2 | B. | C2H4 C3H6 | C. | C3H8 C3H6 | D. | CH4 C2H4 C3H4 |
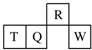 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的非金属性强于Q的非金属性 |
| A. | H2SO4溶于水能形成H+和SO42-,说明H2SO4是离子化合物 | |
| B. | HCl气体溶于水,HCl分子里共价键被破坏 | |
| C. | 单质分子中不存在化学键,化合物分子中才存在化学键 | |
| D. | 含金属元素的离子一定是阳离子 |
| A. | 苏打水 | B. | 白酒 | C. | 柠檬汁 | D. | 纯净水 |
| A. | 0.5mol•L-1•min-1 | B. | 1 mol•L-1•min-1 | ||
| C. | 4 mol•L-1•min-1 | D. | 2 mol•L-1•min-1 |