题目内容
17.有一种有机化合物,其结构简式如图,下列有关它的性质的叙述,正确的是( )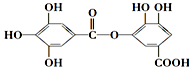
| A. | 有弱酸性,1mol该有机物与溴水反应,最多能消耗4mol Br2 | |
| B. | 在一定条件下,1mol该物质最多能与7mol NaOH完全反应 | |
| C. | 在Ni催化下,1mol该物质可以和8mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
分析 由结构简式可知,该物质中含5个酚-OH、1个-COOH、1个-COOC-,结合酚、羧酸、酯的性质来解答.
解答 解:A.酚羟基的邻、对位氢原子,可以与Br2发生取代反应,所以1 molX最多能与4 molBr2反应,故A正确;
B.在1molZ中含有1mol水解后生成1mol羧基和1mol酚羟基的酯基、1mol羧基、5mol酚羟基,可以和8molNaOH发生反应,故B错误;
C.只有苯环与氢气发生加成反应,则在Ni催化下,1mol该物质可以和6mol H2发生加成反应,故C错误;
D.分子中含有酯基,能发生水解,1mol 有机物水解后能生成2mol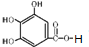 ,故D错误.
,故D错误.
故选A.
点评 本题考查有机物的结构与性质,为高考常见题型,把握物质的官能团及性质的关系为解答的关键,熟悉苯酚、羧酸、酯的性质即可解答,选项BD为易错点,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
8.乙烯可通过石油裂解获得.下列有关乙烯性质的说法错误的是( )
| A. | 在常温常压下为气体 | B. | 不能发生氧化反应 | ||
| C. | 不能自身加成形成聚氯乙烯 | D. | 能使溴的CCl4溶液褪色 |
5.下列装置图对应的实验方案能达到实验目的是( )
| A. | 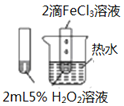 图验证FeCl3对H2O2分解反应有催化作用 | |
| B. | 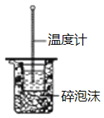 图用于中和热的测定 | |
| C. | 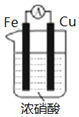 图用于探究Cu作负极的原电池原理 | |
| D. |  图用于比较盐酸、碳酸、硅酸的酸性 |
9.乙酸乙酯和丁酸互为同分异构体,下列方法中不能对二者进行鉴别的是( )
| A. | 利用金属钠 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |
6.设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A. | 标准状况下,22.4 LH2O中含有极性键的数目为2NA | |
| B. | 78 g Na2O2中含有的阴离子数为NA | |
| C. | 11 g重水(D218O)中含有的电子数力5NA | |
| D. | 常温常压下,5.6 g铁粉在7.1 g氯气中充分燃烧,转移的电子数为0.2NA |
7.由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象).阳极上发生的电极反应为2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑;阴极收集到的气体体积为(标准状况)6.72L.
①该电池负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/(mol•L-1) | 0.5 | 2 | 2 | 0.5 |
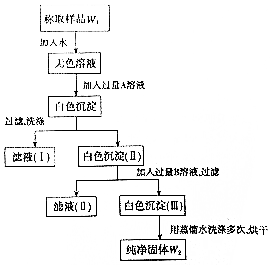 实验室有一瓶已部分被氧化的亚硫酸钠固体,为测定亚硫酸钠的质量分数,某同学设计如图所示实验.请根据实验步骤填写下列空白.
实验室有一瓶已部分被氧化的亚硫酸钠固体,为测定亚硫酸钠的质量分数,某同学设计如图所示实验.请根据实验步骤填写下列空白.