题目内容
20.下面的框图是测定CuSO4•xH2O中结晶水含量的实验流程.(1)填写流程中空白的操作名称:(操作II)和 (操作IV)
(2)其加热装置正确的是A(填编号)
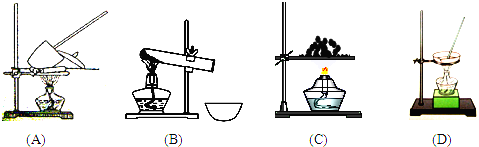
(3)重复操作II、III、IV,直到连续两次称量结果相差不超过0.001g.
(4)现有坩埚、研钵、三角架、泥三角、玻璃棒、干燥器、钥匙、酒精灯(火柴)、硫酸铜晶体样品等试验用品,还缺少的实验用品是天平
操作III必须要在干燥器中(填仪器名称)进行.
(5)以下胆矾结晶水含量的测定操作正确的是C
(A)加热时,晶体溅出坩埚,再加些胆矾
(B)加热时,先用小火,后用大火加热至最后
(C)加热时,不断用玻璃棒搅拌
(6)若实验测得的硫酸铜晶体中结晶水含量偏高,可能的原因有B(选填编号,下同),若实验测得的硫酸铜晶体中结晶水含量偏低,可能的原因有AC.
A.晶体未完全变白就停止加热
B.加热过程中有少量晶体溅出
C.加热后在空气中自然冷却.
分析 (1)测定FeSO4•xH2O中结晶水含量的实验操作包括加热、冷却、称量、恒重;
(2)测定FeSO4•xH2O中结晶水含量的实验中必须在坩埚中加热;
(3)重复操作II、III、IV,直到连续两次称量结果相差不超过0.1g;
(4)实验需要称量固体的质量,操作III冷却为防止空气中的物质和其反应,应在干燥器中冷却;
(5)A.加热时,晶体溅出坩埚,应重新做实验;
B.加热时,先用小火,后用大火加热,至恒重;
C.加热时,不断用玻璃棒搅拌,防止局部受热造成液体飞溅;
(6)A.晶体未完全变白就停止加热,导致结晶水未完全失去;
B.加热过程中有少量晶体溅出,会导致质量差值较大;
C.加热后在空气中自然冷却,会吸收空气中的水重新形成晶体,前后质量差减小.
解答 解:(1)测定FeSO4•xH2O中结晶水含量的实验操作包括加热、冷却、称量、恒重,恒重是为确保硫酸铜晶体完全失去结晶水,故答案为:加热;恒重;
(2 )测定FeSO4•xH2O中结晶水含量的实验中必须在坩埚中加热,装置应选A,故答案为:A;
(3)重复操作II、III、IV,直到连续两次称量结果相差不超过0.001g,故答案为:0.001;
( 4)现有坩埚、研钵、三角架、泥三角、玻璃棒、干燥器、钥匙、酒精灯(火柴)、硫酸铜晶体样品等试验用品,还缺少的实验用品是天平,测定灼烧前后固体的质量;
操作III冷却必须要在干燥器中进行,故答案为:天平;干燥器;
(5)A.加热时,晶体溅出坩埚,应重新做实验,故A错误;
B.加热时,先用小火,后用大火加热,至恒重,故B错误;
C.加热时,不断用玻璃棒搅拌,防止局部受热造成液体飞溅,故C正确;
故答案为:C;
(6)A.加热时间过短而使硫酸铜晶体未完全变白,导致结晶水未完全失去,水的量偏小,则测定结果偏低;
B.加热过程中有少量晶体溅出,会导致质量差值较大,测得结晶水的值偏高;
C.加热后在空气中自然冷却,会吸收空气中的水重新形成晶体,反应前后质量差减小,结果偏低.
故答案为:B;AC.
点评 本题考查物质含量的测定实验,为高频考点,把握反应原理、实验仪器的使用、实验技能等为解答的关键,侧重分析与实验能力的考查,注意结晶水含量的误差分析,题目难度中等.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案(1)可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx$\frac{\underline{\;催化剂\;}}{\;}$(2x+3)N2+6xH2O
某化学兴趣小组模拟该处理过程的实验装置如图1
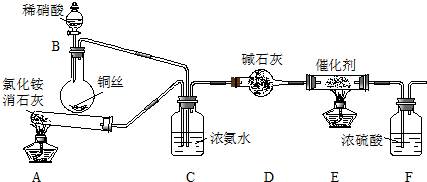
①装置A中发生反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②装置D中碱石灰的作用是除去气体中含有的水蒸气.
(2)用Na2CO3溶液吸收法处理NOx.
已知:NO不能与Na2CO3溶液反应.
NO+NO2+Na2CO3═2NaNO2+CO2 (Ⅰ)
2NO2+Na2CO3═NaNO2+NaNO3+CO2 (Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是D(填字母).
A.1.9 B.1.7 C.1.5 D.1.3
②用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为1.875.
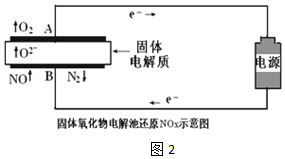
(3)用固体氧化物电解池通过电解方式分解NOx.当以Pt作电极时,固体氧化物电解池还原NO示意图如图2.
298K时,有关实验数据如下,(化学反应消耗的电能占总电能的80%)
| 实验序号 | B极气体 | 电路中通过电子 | 消耗总电能 | 生成N2 |
| 实验1 | NO | 1mol | a KJ | 0.25mol |
| 实验2 | NO和空气 (不考虑NO2) | 1mol | a KJ | 0.09mol |
①根据实验组1数据,NO分解的热化学方程式2NO(g)=N2(g)+O2(g)△H=+3.2akJ•mol-1
②实验组2明显比实验组1生成的N2少,其原因用电极反应式表示为O2+4e-=2O2-或2NO2+8e-=4O2-+N2.
 硒是人体必需的微量元素,它在元素周期表中的位置如图所示.
硒是人体必需的微量元素,它在元素周期表中的位置如图所示.| 磷 | 硫 | ||
| 砷 | 硒 |
a.+99.7kJ•mol-1 b.+29.7kJ•mol-1c.-20.6kJ•mol-1 d.-241.8kJ•mol-1
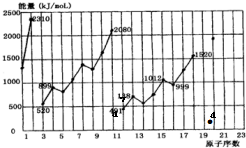
(2)不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如图所示.试根据元素在周期表中的位置,分析图中曲线的变化特点,并回答下列问题.
同周期内,随原子序数增大,E值增大.但个别元素的E值出现反常现象.试预测下列关系式中正确的是ac(填写编号,多选倒扣)
a、E(砷)>E(硒)
b、E(砷)<E(硒)
c、E(溴)>E(硒)
d、E(溴)<E(硒)
估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围419<E<738.
①试管②泥三角③蒸发皿④试管夹⑤坩埚⑥玻璃棒⑦石棉网⑧坩埚钳.
| A. | ①④⑤ | B. | ②⑤⑥⑧ | C. | ②③⑥⑧ | D. | ⑤⑥⑦ |
 (1)CH3-CH3(g)→CH2=CH2(g)+H2(g);有关化学键的键能如下.
(1)CH3-CH3(g)→CH2=CH2(g)+H2(g);有关化学键的键能如下.| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
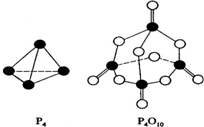
(2)白磷与氧可发生如下反应:P4(S)+5O2(g)=P4O10(S).已知断裂下列化学键需要吸收的能量分别为如下
| 化学键 | P-P | P-O | P=O | O-O | O=O |
| 键能(kJ/mol) | a | b | c | d | e |
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.
已知:①N2(g)+2O2(g)=N2O4 (1)△H1=-195.0kJ•mol-1
②N2H4 (1)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
写出肼和N2O4反应的热化学方程式2N2H4(l)++N2O4(l)=3N2(g)+4H2O(g)△H=-873.4kJ/mol.
| A. | Be | B. | C | C. | Al | D. | Si |
 如图为实验室制备乙烯的装置图,请回答:
如图为实验室制备乙烯的装置图,请回答: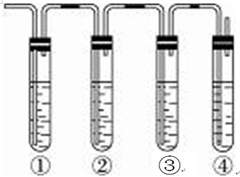 实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫.A.品红溶液 B.NaOH溶液 C.浓硫酸 D.高锰酸钾酸性溶液.试完成下列问题:
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫.A.品红溶液 B.NaOH溶液 C.浓硫酸 D.高锰酸钾酸性溶液.试完成下列问题: