题目内容
已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)△H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l)△H4;
则△H四者的关系中正确的是( )
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g)△H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l)△H4;
则△H四者的关系中正确的是( )
| A、△H1>△H2>△H3>△H4 |
| B、△H4>△H2>△H3>△H1 |
| C、△H3>△H4>△H1>△H2 |
| D、△H4>△H3>△H2>△H1 |
考点:反应热的大小比较
专题:
分析:物质的燃烧是放热的过程,所以焓变都是负值,液态水变为水蒸气需要吸热,据此回答判断.
解答:
解:硫化氢的燃烧过程,完全燃烧生成二氧化硫放出的热多于不完全燃烧生成S单质的热量,所以△H1、△H2<△H3、△H4,液态水变为水蒸气需要吸热,所以△H1>△H2,△H3>△H4,即△H3>△H4>△H1>△H2,故选C.
点评:本题考查学生化学反应的反应热的大小判断知识,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
相关题目
按下列实验方法能够达到要求的是( )
| A、用10mL量筒量取7.50mL稀盐酸 |
| B、用托盘天平称量出25.20g NaCl晶体 |
| C、用pH试纸测得某碱溶液的pH为12.7 |
| D、用25mL碱式滴定管量出14.08mL NaOH溶液 |
下列说法正确的是( )
| A、绿色食品就是颜色为绿色的食品 |
| B、有机食品就是只含有机物的食品 |
| C、维生素C广泛存在于新鲜水果和绿色蔬菜中 |
| D、食盐加碘是在食盐中加KIO3 |
某同学胃部不适,医生诊断后让其服用胃舒平[主要成分有Al(OH)3],度分析下列饮食中,该同学在服药期间不宜食用的是( )
| A、醋 | B、松花蛋 | C、面条 | D、酱油 |
下列离子方程式的书写中,正确的是( )
| A、碳酸氢钙溶液中加入足量烧碱溶液:Ca(HCO3)2+2OH-=CaCO3↓+CO32-+2H2O |
| B、向溴水中通入SO2:Br2+2H2O+SO2=4H++SO42-+2Br- |
| C、向氨水中通过量CO2:2NH3+H2O+CO2=2NH4++CO32-+H2O |
| D、向次氯酸钙溶液中通过少量的SO2:Ca2++2ClO-+SO2=CaSO3↓+2HClO |
下列图示中关于铜电极的连接错误的是( )
A、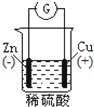 铜锌原电池 |
B、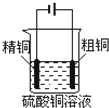 电解精炼铜 |
C、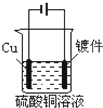 镀件上镀铜 |
D、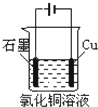 电解氯化铜溶液 |
如图构想的物质循环中太阳能最终转化为( )


| A、化学能 | B、热能 |
| C、生物能 | D、电能 |
实验室中用二氧化锰固体和浓盐酸制备氯气,应选用的下列气体发生装置是( )
A、 |
B、 |
C、 |
D、 |
下列物质的性质比较,正确的是( )
| A、酸性:H2SO4>HClO4>HBrO4 |
| B、碱性:NaOH>KOH>RbOH |
| C、非金属性:P>S>Cl |
| D、半径:S2->Cl->Cl |