题目内容
1.A-J是中学化学中常见的物质,它们之间的转化关系如下框图所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.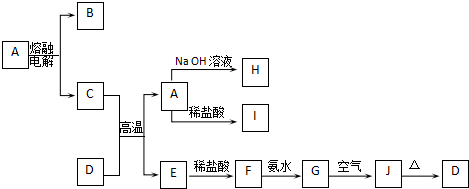
请回答下列问题:
(1)A的化学式为Al2O3,在水中的溶解性难溶(选填“易溶”、“可溶”、“难溶”等).
(2)H溶液中通入过量的CO2,其反应的离子方程式是AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-.
G→J的化学方程式为 4Fe(OH)2+2H2O+O2═4Fe(OH)3.
反应的现象是白色沉淀迅速变成灰绿色,最后变为红褐色.
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因Fe3++3H2O?Fe(OH)3+3H+.
分析 J是一种红褐色沉淀,应为Fe(OH)3,加热分解得到D为Fe2O3,A是一种高熔点物质,能与盐酸、氢氧化钠溶液反应,且电解A得到C与B,则A为Al2O3,故H为NaAlO2,I为AlCl3,在高温下电解氧化铝生成Al与氧气,C能与D(氧化铁)反应生成A与E,可推知C为Al、B为O2,E为Fe,由转化转化关系可知F为FeCl2,G为Fe(OH)2,据此解答.
解答 解:J是一种红褐色沉淀,应为Fe(OH)3,加热分解得到D为Fe2O3,A是一种高熔点物质,能与盐酸、氢氧化钠溶液反应,且电解A得到C与B,则A为Al2O3,则H为NaAlO2,I为AlCl3,在高温下电解氧化铝生成Al与氧气,C能与D(氧化铁)反应生成A与E,可推知C为Al、B为O2,E为Fe,由转化转化关系可知F为FeCl2,G为Fe(OH)2,
(1)由上述分析可知,A为Al2O3,难溶于水,故答案为:Al2O3;难溶;
(2)H为NaAlO2,其溶液中通入过量的CO2的离子方程式是:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
G→J是氢氧化亚铁氧化生成氢氧化铁,化学方程式为:4Fe(OH)2+2H2O+O2═4Fe(OH)3,反应现象是:白色沉淀迅速变成灰绿色,最后变为红褐色,
故答案为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;4Fe(OH)2+2H2O+O2═4Fe(OH)3;白色沉淀迅速变成灰绿色,最后变为红褐色;
(3)D(Fe)物质恰好溶于一定量的稀盐酸后生成氯化铁溶液,溶液中Fe3+水解:Fe3++3H2O?Fe(OH)3+3H+,破坏水的电离平衡,溶液显酸性,
故答案为:Fe3++3H2O?Fe(OH)3+3H+.
点评 本题考查无机物的推断,J的颜色及A的性质是推断突破口,涉及常见金属及其化合物的性质,侧重对化学用语的考查,有一定的综合性,难度中等.

| A. | 简单离子半径:Z>Y | B. | 阳离子的氧化性:X>Z | ||
| C. | 氧化物对应水化物的酸性:R>W | D. | X和Y只能形成一种化合物 |
| A. | 形成化学键 | B. | 燃料燃烧 | ||
| C. | 化合反应 | D. | 葡萄糖在体内的氧化分解 | ||
| E. | 酸碱中和 | F. | 炸药爆炸 |
| A. | HCl、Na2CO3 | B. | AlCl3、NaOH | C. | NaAlO2、HCl | D. | MgCl2、AgNO3 |
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 9种 |
| A. | 由红色变为深红色 | B. | 由无色变为深红色 | ||
| C. | 由浅红色变成深红色 | D. | 由无色变为浅红色 |
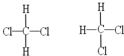 ②O2、O3③H2O、D2O
②O2、O3③H2O、D2O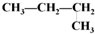 、CH3-CH2-CH3.
、CH3-CH2-CH3.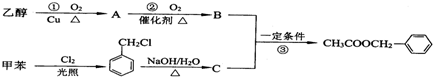
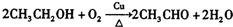 .
. .
.