题目内容
14.(1)欲用18.4mol/L的浓硫酸配制成浓度为0.5mol/L的稀硫酸500ml,量筒应选用15mL的量筒最好(从10mL、15mL、20mL选填),量取时发现量筒不干净用水洗净后直接量取将使浓度偏低(填“偏高”、“偏低”或“无影响”)
(2)向沸水中逐滴加入5滴~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,得到的分散系即为Fe(OH)3胶体,反应的化学方程式为:FeCl3+3H2O=Fe(OH)3(胶体)+3HCl.
(3)向NaHSO4溶液中滴入Ba(OH)2溶液至中性,请写出此步反应的离子方程式2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O此时的溶液中溶质为:Na2SO4(填化学式)
分析 (1)依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸体积,据此选择容量瓶规格;量取时发现量筒不干净用水洗净后直接量取实质将溶液稀释,据此解答;
(2)氯化铁水解生成氢氧化铁胶体,溶液出现透明的红褐色;
(3)向NaHSO4溶液中滴入Ba(OH)2溶液至中性,二者物质的量之比为2:1,据此书写方程式,依据方程式判断反应后溶液溶质成分.
解答 解:(1)解:设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变计算得:18.4mol/L×V=
0.5mol/L×500mL,解得V=13.6mL,应选择15mL量筒;量取时发现量筒不干净用水洗净后直接量取实质将溶液稀释,所以溶液浓度偏低;
故答案为:15;偏低;
(2)氯化铁水解生成氢氧化铁胶体,水方程式为:FeCl3+3H2O=Fe(OH)3(胶体)+3HCl,溶液出现透明的红褐色;
故答案为:红褐色; FeCl3+3H2O=Fe(OH)3(胶体)+3HCl;
(3)向NaHSO4溶液中滴入Ba(OH)2溶液至中性,二者物质的量之比为2:1,化学方程式:2NaHSO4+2Ba(OH)2=BaSO4↓+2H2O,反应离子方程式:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O;反应后溶质为:硫酸钠,化学式为:Na2SO4;
故答案为:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O; Na2SO4.
点评 本题考查了一定物质的量浓度溶液的配制和离子方程式书写,明确溶液稀释规律及量筒规格选择依据,熟悉氢氧化铁胶体制备过程是解题关键,题目难度不大.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
5.一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)?Y(g)+Z(s),以下不能作为反应达到平衡标志的是( )
| A. | X的分解速率是Y的消耗速率的2倍 | |
| B. | 混合气体的压强不再变化 | |
| C. | 单位时间内生成l mol Y的同时分解2 mol X | |
| D. | 混合气体的密度不再变化 |
2. 研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
(1)生产水煤气过程中有以下反应:
①C(s)+CO2(g)?2CO(g)△H1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3;
若平衡表达式为K=$\frac{c(H_{2})•c(CO)}{c(H_{2}O)}$,则它所对应的化学反应方程式是(填序号)③.
(2)对反应①下列说法中能说明该反应达到平衡状态的bcd
a.温度和体积一定时,混合气体的颜色不再变化
b.温度和体积一定时,容器内的压强不再变化
c.温度和体积一定时,生成物的浓度不再变化
d.温度和体积一定时,混合气体的密度不再变化
(3)不同温度下反应②的平衡常数如下表所示.则△H2<0(填“<”或“>”);在500℃时,把等物质的量浓度的CO和H2O(g)充入反应容器,达到平衡时c(CO)=0.005mol•L-1、c(H2)=0.015mol•L-1,则CO的平衡转化率为75%.
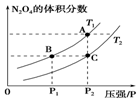
(4)对反应2NO2(g)?N2O4(g)△H<0在温度为T1、T2时,平衡体系N2O4的体积分数随压强变化曲线如图所示.
则T1<T2(填“>”或“<”);增大压强,平衡正反应方向移动(填“正反应方向”或“逆反应方
向”或“不”); B、C两点的平衡常数B>C(填“>”或“<”).
 研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:(1)生产水煤气过程中有以下反应:
①C(s)+CO2(g)?2CO(g)△H1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3;
若平衡表达式为K=$\frac{c(H_{2})•c(CO)}{c(H_{2}O)}$,则它所对应的化学反应方程式是(填序号)③.
(2)对反应①下列说法中能说明该反应达到平衡状态的bcd
a.温度和体积一定时,混合气体的颜色不再变化
b.温度和体积一定时,容器内的压强不再变化
c.温度和体积一定时,生成物的浓度不再变化
d.温度和体积一定时,混合气体的密度不再变化
(3)不同温度下反应②的平衡常数如下表所示.则△H2<0(填“<”或“>”);在500℃时,把等物质的量浓度的CO和H2O(g)充入反应容器,达到平衡时c(CO)=0.005mol•L-1、c(H2)=0.015mol•L-1,则CO的平衡转化率为75%.
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.945795506 | 9 | 1 |
则T1<T2(填“>”或“<”);增大压强,平衡正反应方向移动(填“正反应方向”或“逆反应方
向”或“不”); B、C两点的平衡常数B>C(填“>”或“<”).
6.已知X、Y元素同周期,且电负性X>Y,下列说法正确的是( )
| A. | 第一电离能:Y小于X | |
| B. | 气态氢化物的稳定性:HmY强于HnX | |
| C. | 最高价含氧酸的酸性X弱于Y | |
| D. | X和Y形成化合物时,X显负价Y显正价 |
 .
.
 .
.