题目内容
11.KI在食品、医药领域有广泛用途.某科研小组利用碘废弃液(主要含I2、I-)制备KI,流程如下: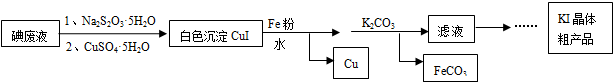
已知:I2+2S2O32-=S4O62-+2I-
(1)加入胆矾的作用氧化剂,富集碘元素.
(2)为制得KI晶体粗产品,滤液后续操作步骤是将滤液倒入蒸发皿中加热蒸发、冷却结晶,过滤、干燥得到KI晶体粗产品.
(3)用沉淀滴定法测定样品中KI含量的实验步骤如下:
a.称取3.000g样品,溶解,配制成250mL溶液
b.量取25.00mL待测液于锥形瓶中;
c.用0.1000mol•L-1AgNO3标准溶液滴定至终点,记录消耗AgNO3标准溶液的体积;
d.重复b、c操作2~3次,平均消耗AgNO3标准溶液16.50mL
①配制250mL样品溶液时,所需的仪器除烧杯、玻璃棒之外,还缺少的玻璃仪器是
250ml容量瓶、胶头滴管.
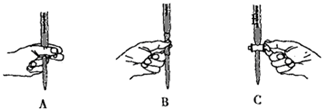
②AgNO3标准溶液在使用之前通常要重新标定,原因是硝酸银不稳定,见光易分解,放置之后的硝酸银溶液的浓度会发生变化;本实验滴定过程中操作滴定管的图示正确的是A(填编号).
③该样品中KI的质量百分数为91.30%.
④下列因素会导致KI含量的测定结果偏高的是C.
A.配制样品溶液定容时仰视 B.锥形瓶未干燥
C.滴定管未用AgNO3标准溶液润洗 D.滴定终点时滴定管尖嘴中产生气泡.
分析 (1)由流程图可知硫酸铜被还原成碘化亚铜沉淀,从而富集碘元素;
(2)从溶液中得到溶质,通常采取蒸发、浓缩、冷却结晶、过滤、干燥方法;
(3)①根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
②根据硝酸银不稳定,见光易分解;根据酸式滴定管的使用方法;
③根据关系式:AgNO3~KI来计算出碘化钾的质量,从而求出含量;
④根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差.
解答 解:(1)由流程图可知硫酸铜被还原成碘化亚铜沉淀,硫酸铜晶体作氧化剂,富集碘元素;
故答案为:氧化剂,富集碘元素;
(2)为制得KI晶体粗产品,将滤液倒入蒸发皿中加热蒸发、冷却结晶,过滤、干燥得到KI晶体粗产品;
故答案为:将滤液倒入蒸发皿中加热蒸发、冷却结晶,过滤、干燥得到KI晶体粗产品
(3)①实验室要250mL待测溶液,用天平和药匙称取3.000g样品,在烧杯中溶解(可用量筒量取水),冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管,所需的仪器除烧杯、玻璃棒之外,还缺少的玻璃仪器是有250ml容量瓶、胶头滴管;
故答案为:250ml容量瓶、胶头滴管;
②硝酸银不稳定,见光易分解,放置之后的硝酸银溶液的浓度会发生变化,对滴定结果造成影响,需要重新标定;使用酸式滴定管时,左手握滴定管,其无名指和小指向手心弯曲,轻轻地贴着出口部分,用其余三指控制活塞的转动;
故答案为:硝酸银不稳定,见光易分解,放置之后的硝酸银溶液的浓度会发生变化;A;
③滴定消耗的AgNO3的物质的量为0.1000mol•L-1×0.01650L=0.001650mol,由关系式AgNO3~KI可知25.00mL待测液中含有0.001650molKI,250mL溶液中含有0.01650molKI,即0.01650mol×166g/mol=2.739g,该样品中KI的质量百分数为$\frac{2.739g}{3.000g}$×100%=91.30%;
故答案为:91.30%;
④A.配制样品溶液定容时仰视,对实验无影响,故A错误;
B.锥形瓶未干燥,待测液的物质的量不变,测定结果不变,故B错误;
C.滴定管未用AgNO3标准溶液润洗,溶液被稀释,导致V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)偏大,KI的质量偏大,含量也偏大,故C正确;
D.滴定终点时滴定管尖嘴中产生气泡,导致V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,可知c(待测)偏小,KI的质量偏小,含量也偏小;
故选C.
点评 本题考查了物质的制备与组成含量测定等,涉及滴定操作、滴定应用与计算等,难度中等,注意滴定中经常根据关系式进行计算,掌握根据关系式计算方法.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,SO2的转化率:α1<80%<α2 | |
| D. | 平衡时,丙中气体平均相对分子质量与甲相同 |
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
探究浓度对化学反应速率的影响,应选择①②或①③或④⑤(填实验编号);
若同时选择①②③溶液变浑浊的时间,探究比较改变不同反应物浓度对反应速率的影响对化学反应速率的影响.
反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2;
在不同温度时K1、K2的值如表:
| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
②能判断CO2(g)+H2(g)?CO(g)+H2O(g)达到化学平衡状态的依据是BC(填序号).
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.将体积比为1:2的CO2、H2气体置于密闭容器中发生上述反应,CO和H2O的体积比保持不变时.
| A. | 有4种不同的伸展方向 | B. | 有5种不同能量的电子 | ||
| C. | 有5种不同的运动范围 | D. | 有14种不同运动状态的电子 |
| A. | 无变化 | B. | 颜色变浅 | C. | 变为棕黄色 | D. | 变为红褐色 |
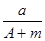 (A-N+m)mol B.
(A-N+m)mol B. 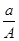 (A-N)mol
(A-N)mol