题目内容
铝分别于足量的稀盐酸和氢氧化钠溶液反应,当反应中消耗的HCl和NaOH的物质的量相等时,两个反应放出的气体在标准状况下体积之比为( )
| A、1:1 | B、2:1 |
| C、1:3 | D、3:1 |
考点:化学方程式的有关计算,铝的化学性质
专题:计算题
分析:铝与盐酸发生反应:2Al+6HCl=2AlCl3+3H2↑,铝与NaOH溶液发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,假设消耗的HCl和NaOH的物质的量都是6mol,根据方程式计算生成氢气的物质的量,相同条件下,气体的体积之比等于其物质的量之比.
解答:
解:假设消耗的HCl和NaOH的物质的量都是6mol,则:
2Al+6HCl=2AlCl3+3H2↑
6mol 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
6mol 9mol
相同条件下,气体的体积之比等于其物质的量之比,故生成氢气的体积之比=3mol:9mol=1:3,
故选C.
2Al+6HCl=2AlCl3+3H2↑
6mol 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
6mol 9mol
相同条件下,气体的体积之比等于其物质的量之比,故生成氢气的体积之比=3mol:9mol=1:3,
故选C.
点评:本题考查化学方程式的有关计算,比较基础,明确发生的反应是关键,注意利用赋值法解答.

练习册系列答案
相关题目
在水溶液中的电离方程式正确的是( )
| A、NaHSO4=Na++HSO4- |
| B、NaHCO3?Na++HCO3- |
| C、MgCl2═Mg2++Cl2- |
| D、Ba(OH)2═Ba2++2OH- |
下列说法正确的是( )
| A、在101kPa下,1g物质完全燃烧所放出的热量叫该物质的热值,单位为kJ?mol-1 | ||
| B、某放热反应在其它条件不变时,加入催化剂后反应放出的热量会减少 | ||
| C、一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的 | ||
D、若一个反应的焓变△H=a kJ?mol-1,则其逆反应△H=
|
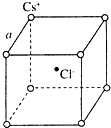 如图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为a cm,氯化铯(CsCl)的相对分子质量M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为a cm,氯化铯(CsCl)的相对分子质量M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )A、
| ||
B、
| ||
C、
| ||
D、
|
下列装置中能组成原电池形成电流的是( )
A、 |
B、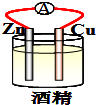 |
C、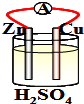 |
D、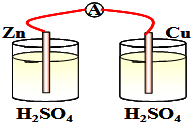 |
一种由甲醇(CH3OH)和氧气以及氢氧化钠做电解质溶液的新型电池,其两极的电极反应式为:2CH3 OH+16OH--12e-=2CO32-+12H2O,6H2O+3O2+12e-=12OH-,关于此电池的推断正确的是( )
| A、通入氧气的一极是负极 |
| B、放电时,溶液中的OH-向正极移动 |
| C、反应中若有6mol电子发生转移,则有32g CH3 OH被还原 |
| D、该电池工作时甲醇一极附近溶液的pH降低 |
下列离子或分子在溶液中能大量共存,通入SO2后仍能大量共存的一组是( )
| A、K+、Cl-、NO3-、Ca2+ |
| B、NH4+、Cl-、Na+、SO42- |
| C、H+、Fe2+、SO32-、Br2 |
| D、AlO2-、NH3?H2O、Na+、Ag+ |
在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20gA与一定量B恰好完全反应,生成5gD,则在此反应中B和C的质量比为( )
| A、4:19 | B、3:5 |
| C、1:3 | D、2:17 |
能表示阿伏加德罗常数数值的是( )
| A、1 mol 金属钠含有的电子数 |
| B、标准状况下,22.4 L 苯所含的分子数 |
| C、0.012 kg 12C所含的原子数 |
| D、1 L 1 mol?L-1硫酸溶液所含的H+数 |