题目内容
向100ml1mol/L的MCln 溶液中加入1mol/L的AgNO3溶液300ml恰好完全反应,则n= .原溶液中Cl-的物质的量的浓度为 mol/L.
考点:物质的量浓度的相关计算
专题:计算题
分析:发生反应Ag++Cl-=AgCl↓,二者恰好完全反应则n(Ag+)=n(Cl-),据此计算n的值、氯离子物质的量,再根据c=
计算氯离子物质的量浓度.
| n |
| V |
解答:
解:发生反应Ag++Cl-=AgCl↓,二者恰好完全反应则:n(Cl-)=n(Ag+)=0.3L×1mol/L=0.3mol,
故n×0.1L×1mol/L=0.3mol,则n=3,c(Cl-)=
=3mol/L,
故答案为:3;3.
故n×0.1L×1mol/L=0.3mol,则n=3,c(Cl-)=
| 0.3mol |
| 0.1L |
故答案为:3;3.
点评:本题考查离子方程式计算、物质的量浓度计算,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
下列物质:①MgCl2 ②SiO2 ③白磷 ④BF3 ⑤NH3 ⑥四氯化碳 其中含极性键的非极性分子是( )
| A、①②③④⑥ | B、①④⑤⑥ |
| C、③④⑥ | D、④⑥ |
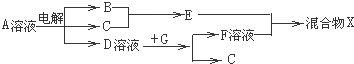
强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32-、SO32-、SO42-、C1-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:下列结论正确的是( )


| A、X中不能确定的离子是 A13+、Na+、K+和C1- |
| B、气体F经催化氧化可直接生成气体D |
| C、沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 |
| D、X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- |
下列反应的离子方程式书写正确的是( )
| A、铝与稀硫酸反应:Al+2H+=Al3++H2↑ |
| B、碳酸钙与稀盐酸的反应:CO32-+2H+=CO2+H2O |
| C、氨水与盐酸反应:OH-+H+=H2O |
| D、实验室用氢氧化钠溶液吸收多余的Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
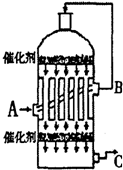 硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
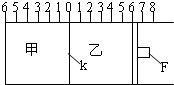 Ⅰ.如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题:
Ⅰ.如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题: