题目内容
 喀麦隆的“杀人湖”(尼奥斯湖)曾于1986年使1800多名附近居民在一夜之间神秘死去.后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体并发现在200m深的湖底,每立方米湖水竟溶解8m3的有毒气体,目前科技人员已找到一种有效的办法将湖底的有毒气体抽出并加以处理.回答:
喀麦隆的“杀人湖”(尼奥斯湖)曾于1986年使1800多名附近居民在一夜之间神秘死去.后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体并发现在200m深的湖底,每立方米湖水竟溶解8m3的有毒气体,目前科技人员已找到一种有效的办法将湖底的有毒气体抽出并加以处理.回答:(1)为了测定从湖底取出的水样中SO2的含量.可在一定量的水样中加入一定量的碘(过量),再用已知浓度的硫代硫酸钠溶液滴定过量的碘.该反应为:2Na2S203+I2═Na2S406+2NaI
①碘和水样中S02反应的化学方程式为
②用硫代硫酸钠滴定过量的碘时.应用
③若在20mL的水样中加入碘Wg,用去VmLCmol/L的Na2S2O3溶液,则水样中S02浓度为
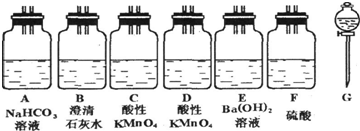
(2)为了测定从湖底抽出的有毒气体中C02的含量,需将C02变成沉淀,然后测其质量,通过计算求出C02的含量.从图中选择必要的装置(导管和胶管省略):设计实验,将C02转变成沉淀.
①其所选装置的连接顺序是(按从上到下从左到右的顺序)
②将气体2次通过酸性高锰酸钾溶液的目的是
③是否需要选择装置B.原因是
④为了得到沉淀物的质量还需进行的操作有
考点:探究物质的组成或测量物质的含量
专题:
分析:(1)①碘单质具有氧化性氧化二氧化硫为硫酸,结合原子守恒配平书写;
②碘单质遇到淀粉变蓝,硫代硫酸钠和和碘单质反应,蓝色褪去,终点判断是蓝色褪去且半分钟不变化这么反应达到终点;
③由2Na2S2O3+I2═2NaI+Na2S4O6
2 mol 254 g
cV×10-3 mol 127×10-3cV g
得与SO2反应的I2的质量m(I2)=W g-127×10-3cV g,再依据
I2+SO2+2H2O═H2SO4+2HI
254 g 1 mol
m(I2)
mol
得到水样中c(SO2)=
=
=(
-
)mol/L;
(2)①二氧化碳和二氧化硫等有毒气体,为了测定从湖底抽出的有毒气体中C02的含量,需将C02变成沉淀,然后测其质量,设计实验,将C02转变成沉淀,实验设计碳酸氢钠溶液中加入水样,二氧化硫被碳酸氢钠溶液吸收,同时是二氧化碳气体,再通过装置CD除去毒气S02,并确认S02已经除尽,通过氢氧化钡溶液吸收生成的二氧化碳气体,最后通过装置F防止空气中二氧化碳和水蒸气进入装置E干扰实验结果;
②两次通过高锰酸钾溶液是为了除净二氧化硫和检验是否除净的作用;
③装置B中氢氧化钙溶解度小,反应过程中二氧化碳气体是水样中和二氧化硫与碳酸氢钠反应生成的二氧化碳总和;
④得到沉淀物的质量,需要过滤、洗涤、干燥、称量至恒重;需要过滤装置、洗涤装置、干燥装置和称量仪器.
②碘单质遇到淀粉变蓝,硫代硫酸钠和和碘单质反应,蓝色褪去,终点判断是蓝色褪去且半分钟不变化这么反应达到终点;
③由2Na2S2O3+I2═2NaI+Na2S4O6
2 mol 254 g
cV×10-3 mol 127×10-3cV g
得与SO2反应的I2的质量m(I2)=W g-127×10-3cV g,再依据
I2+SO2+2H2O═H2SO4+2HI
254 g 1 mol
m(I2)
| m(I2) |
| 254 |
得到水样中c(SO2)=
| m(I2) |
| 254×20×10-3 |
| W-127×10-3cV |
| 254×20×10-3 |
| W |
| 5..08 |
| cV |
| 40 |
(2)①二氧化碳和二氧化硫等有毒气体,为了测定从湖底抽出的有毒气体中C02的含量,需将C02变成沉淀,然后测其质量,设计实验,将C02转变成沉淀,实验设计碳酸氢钠溶液中加入水样,二氧化硫被碳酸氢钠溶液吸收,同时是二氧化碳气体,再通过装置CD除去毒气S02,并确认S02已经除尽,通过氢氧化钡溶液吸收生成的二氧化碳气体,最后通过装置F防止空气中二氧化碳和水蒸气进入装置E干扰实验结果;
②两次通过高锰酸钾溶液是为了除净二氧化硫和检验是否除净的作用;
③装置B中氢氧化钙溶解度小,反应过程中二氧化碳气体是水样中和二氧化硫与碳酸氢钠反应生成的二氧化碳总和;
④得到沉淀物的质量,需要过滤、洗涤、干燥、称量至恒重;需要过滤装置、洗涤装置、干燥装置和称量仪器.
解答:
解:(1)①碘和水样中S02反应的化学方程式为:I2+S02+2H20=H2SO4+2HI,故答案为:I2+S02+2H20=H2SO4+2HI;
②用硫代硫酸钠滴定过量的碘时,碘单质遇到淀粉变蓝,硫代硫酸钠和和碘单质反应,蓝色褪去,终点判断是蓝色褪去且半分钟不变化这么反应达到终点;
故答案为:淀粉溶液,蓝色刚好褪去;
③由2Na2S2O3+I2═2NaI+Na2S4O6
2 mol 254 g
cV×10-3 mol 127×10-3cV g
得与SO2反应的I2的质量m(I2)=W g-127×10-3cV g,再依据
I2+SO2+2H2O═H2SO4+2HI
254 g 1 mol
m(I2)
mol
得到水样中c(SO2)=
=
=(
-
)mol/L,
故答案为:
-
;
(2)①二氧化碳和二氧化硫等有毒气体,为了测定从湖底抽出的有毒气体中C02的含量,需将C02变成沉淀,然后测其质量,设计实验,将C02转变成沉淀,实验设计碳酸氢钠溶液中加入水样,二氧化硫被碳酸氢钠溶液吸收,同时是二氧化碳气体,再通过装置CD除去毒气S02,并确认S02已经除尽,通过氢氧化钡溶液吸收生成的二氧化碳气体,最后通过装置F防止空气中二氧化碳和水蒸气进入装置E干扰实验结果,其所选装置的连接顺序是G A C D E F;
故答案为:G A C D E F;
②两次通过高锰酸钾溶液是为了除净二氧化硫和检验是否除净的作用,所以第一次是为了除去毒气S02,第二次为了确认S02已经除尽;
故答案为:第一次是为了除去毒气S02,第二次为了确认S02已经除尽;
③装置B中氢氧化钙溶解度小,反应过程中二氧化碳气体是水样中和二氧化硫与碳酸氢钠反应生成的二氧化碳总和,不需要B装置,因为气体通过NaHC03溶液S02与NaHCO3反应生成C02,改变了原气体的C02的量.
故答案为:不需要,因为气体通过NaHC03溶液S02与NaHCO3反应生成C02,改变了原气体的C02的量;
④得到沉淀物的质量,需要过滤、洗涤、干燥、称量至恒重;需要过滤装置、洗涤装置、干燥装置和称量仪器,主要有铁架台,漏斗,玻璃棒,烧杯,干燥器,天平;
故答案为:过滤,洗涤,干燥,称量;铁架台,漏斗,玻璃棒,烧杯,干燥器,天平.
②用硫代硫酸钠滴定过量的碘时,碘单质遇到淀粉变蓝,硫代硫酸钠和和碘单质反应,蓝色褪去,终点判断是蓝色褪去且半分钟不变化这么反应达到终点;
故答案为:淀粉溶液,蓝色刚好褪去;
③由2Na2S2O3+I2═2NaI+Na2S4O6
2 mol 254 g
cV×10-3 mol 127×10-3cV g
得与SO2反应的I2的质量m(I2)=W g-127×10-3cV g,再依据
I2+SO2+2H2O═H2SO4+2HI
254 g 1 mol
m(I2)
| m(I2) |
| 254 |
得到水样中c(SO2)=
| m(I2) |
| 254×20×10-3 |
| W-127×10-3cV |
| 254×20×10-3 |
| W |
| 5..08 |
| cV |
| 40 |
故答案为:
| W |
| 5..08 |
| cV |
| 40 |
(2)①二氧化碳和二氧化硫等有毒气体,为了测定从湖底抽出的有毒气体中C02的含量,需将C02变成沉淀,然后测其质量,设计实验,将C02转变成沉淀,实验设计碳酸氢钠溶液中加入水样,二氧化硫被碳酸氢钠溶液吸收,同时是二氧化碳气体,再通过装置CD除去毒气S02,并确认S02已经除尽,通过氢氧化钡溶液吸收生成的二氧化碳气体,最后通过装置F防止空气中二氧化碳和水蒸气进入装置E干扰实验结果,其所选装置的连接顺序是G A C D E F;
故答案为:G A C D E F;
②两次通过高锰酸钾溶液是为了除净二氧化硫和检验是否除净的作用,所以第一次是为了除去毒气S02,第二次为了确认S02已经除尽;
故答案为:第一次是为了除去毒气S02,第二次为了确认S02已经除尽;
③装置B中氢氧化钙溶解度小,反应过程中二氧化碳气体是水样中和二氧化硫与碳酸氢钠反应生成的二氧化碳总和,不需要B装置,因为气体通过NaHC03溶液S02与NaHCO3反应生成C02,改变了原气体的C02的量.
故答案为:不需要,因为气体通过NaHC03溶液S02与NaHCO3反应生成C02,改变了原气体的C02的量;
④得到沉淀物的质量,需要过滤、洗涤、干燥、称量至恒重;需要过滤装置、洗涤装置、干燥装置和称量仪器,主要有铁架台,漏斗,玻璃棒,烧杯,干燥器,天平;
故答案为:过滤,洗涤,干燥,称量;铁架台,漏斗,玻璃棒,烧杯,干燥器,天平.
点评:本题考查了物质组成的实验探究和实验验证方法分析判断,含量计算应用,实验基本操作的分析判断,氧化还原反应定量计算应用,掌握过程分析和方法应用时关键,题目难度较大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列说法中正确的是( )
| A、非金属原子组成的化合物不可能是离子化合物 |
| B、ⅠA族元素的金属性一定比ⅡA族元素的金属性强 |
| C、同一主族元素组成的化合物一定是共价化合物 |
| D、NH4H中的所有原子的最外层都符合相应稀有气体原子电子层结构,1mol NH5中含有4NA个N-H键(NA表示阿伏加德罗常数的值) |
下列各物质既能发生消去反应生成相应的烯烃,又能氧化成相应的醛的是( )
| A、CH3OH |
| B、(CH3)3COH |
| C、CH3CHOHCH3 |
| D、CH3CH2CH2OH |
用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A、1mol金刚石中含有C-C键的数目为4NA |
| B、14克N2中含有的π键数目为NA |
| C、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| D、1L0.1mol/LAl2(SO4)3溶液中含有的Al3+总数为0.2NA |

 和
和 ,应选用
,应选用 ,
,